
 在測定空氣里氧氣含量的實驗中:在集氣瓶內加入少量的水,并做上標記,余 下的容積五等分.用彈簧夾夾住乳膠管.點燃紅磷伸入瓶中并塞上瓶塞.待紅磷熄滅并冷卻后,打開彈簧夾,觀察廣口瓶內水面變化情況.實驗完畢甲、乙、丙同學觀察到不同的現象.
在測定空氣里氧氣含量的實驗中:在集氣瓶內加入少量的水,并做上標記,余 下的容積五等分.用彈簧夾夾住乳膠管.點燃紅磷伸入瓶中并塞上瓶塞.待紅磷熄滅并冷卻后,打開彈簧夾,觀察廣口瓶內水面變化情況.實驗完畢甲、乙、丙同學觀察到不同的現象. ;
; ;
; .
. 2P2O5
2P2O5

科目:初中化學 來源: 題型:
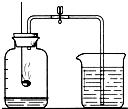 在測定空氣里氧氣含量的實驗中:在集氣瓶內加入少量的水,并做上標記,余 下的容積五等分.用彈簧夾夾住乳膠管.點燃紅磷伸入瓶中并塞上瓶塞.待紅磷熄滅并冷卻后,打開彈簧夾,觀察廣口瓶內水面變化情況.實驗完畢甲、乙、丙同學觀察到不同的現象.
在測定空氣里氧氣含量的實驗中:在集氣瓶內加入少量的水,并做上標記,余 下的容積五等分.用彈簧夾夾住乳膠管.點燃紅磷伸入瓶中并塞上瓶塞.待紅磷熄滅并冷卻后,打開彈簧夾,觀察廣口瓶內水面變化情況.實驗完畢甲、乙、丙同學觀察到不同的現象.| 1 |
| 5 |
| 1 |
| 5 |
| 1 |
| 5 |
查看答案和解析>>
科目:初中化學 來源: 題型:
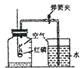 如圖所示,在“測定空氣里氧氣含量”的實驗中,紅磷燃燒的化學方程式為
如圖所示,在“測定空氣里氧氣含量”的實驗中,紅磷燃燒的化學方程式為
| ||
| ||
| 1 |
| 5 |
查看答案和解析>>
科目:初中化學 來源: 題型:
| 1 | 5 |
查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
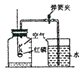 如圖所示,在“測定空氣里氧氣含量”的實驗中,紅磷燃燒的化學方程式為________;若測紅磷燃燒一段時間后自動熄滅,從燃燒條件看是由于________,若測定出O2的含量小于空氣體積的
如圖所示,在“測定空氣里氧氣含量”的實驗中,紅磷燃燒的化學方程式為________;若測紅磷燃燒一段時間后自動熄滅,從燃燒條件看是由于________,若測定出O2的含量小于空氣體積的 ,原因可能是________.(寫一條即可)
,原因可能是________.(寫一條即可)查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com