
| 稀鹽酸的總質量(g) | 10.00 | 20.00 | 30.00 | 40.00 | 50.00 | 60.00 | 70.00 |
| 燒杯中物質總質量(g) | 14.66 | 24.22 | m | 43.34 | 52.90 | 62.90 | 72.90 |
分析 (1)利用相對分子質量等于各元素相對原子質量的和即可求得碳酸鈣的相對分子質量;
(2)由表中數據可知,當加入的稀鹽酸是10g、20g時,其中的碳酸鈣能和稀鹽酸完全反應,而加入的稀鹽酸是60g時,碳酸鈣完全反應,而稀鹽酸有剩余,且生成二氧化碳的質量為60g+5.1g-62.90g=2.20g,每加入10g稀鹽酸生成二氧化碳的質量=10g+5.1g-14.66g=0.44g
所以當加入30g稀鹽酸時,碳酸鈣和稀鹽酸也完全反應,m=30g+5.1g-0.44g×3=33.78g
(3)根據生成的二氧化碳的質量計算該石灰石礦中碳酸鈣的質量;
解答 解:(1)碳酸鈣的化學式為:CaCO3,故碳酸鈣的相對分子質量為:40+12+16×3=100;故填:100;
(2)由表中數據可知,當加入的稀鹽酸是10g、20g時,其中的碳酸鈣能和稀鹽酸完全反應,而加入的稀鹽酸是60g時,碳酸鈣完全反應,而稀鹽酸有剩余,且生成二氧化碳的質量為60g+5.1g-62.90g=2.20g,每加入10g稀鹽酸生成二氧化碳的質量=10g+5.1g-14.66g=0.44g
所以當加入30g稀鹽酸時,碳酸鈣和稀鹽酸也完全反應,m=30g+5.1g-0.44g×3=33.78g
(2)設4克石灰石中含有碳酸鈣的質量為x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.20g
$\frac{100}{x}=\frac{44}{2.20g}$
x=5.00g
樣品中碳酸鈣的質量分數=$\frac{5.00g}{5.10g}×$100%≈98.04%.
答案:
(1)100;
(2)33.78;
(3)樣品中碳酸鈣的質量分數為98.04%.
點評 本題主要考查學生運用假設法和化學方程式進行計算和推斷的能力,書寫化學方程式要注意配平,計算步驟要注意規范性.


科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 兒茶素中含有3種元素 | |
| B. | 兒茶素中碳的質量分數為58.4% | |
| C. | 兒茶素分子中碳和氫的原子個數比為15:14 | |
| D. | 兒茶素是一種有機物 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
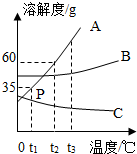 (1)現有H、O、Na、Mg、P五種元素,請根據下列要求寫出由所給元素組成的物質(寫化學式):
(1)現有H、O、Na、Mg、P五種元素,請根據下列要求寫出由所給元素組成的物質(寫化學式):查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
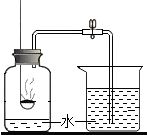 用紅磷燃燒測定空氣中氧氣含量的實驗裝置如圖所示,實驗過程中,下列做法會使實驗結果產生明顯誤差的是( )
用紅磷燃燒測定空氣中氧氣含量的實驗裝置如圖所示,實驗過程中,下列做法會使實驗結果產生明顯誤差的是( )| A. | 使用過量的紅磷 | |
| B. | 把紅磷改為蠟燭 | |
| C. | 恢復到實驗開始前的溫度才進行測量 | |
| D. | 不打開橡膠塞,用放大鏡聚焦太陽光點燃紅磷 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
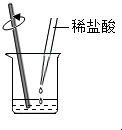 用化學方法可制取純凈的物質,化學興趣小組應用中和反應原理制取氯化鈉固體.
用化學方法可制取純凈的物質,化學興趣小組應用中和反應原理制取氯化鈉固體.查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 濃鹽酸具有揮發性所以濃硫酸也具有揮發性 | |
| B. | 某固體中加入稀鹽酸,生成無色無味的氣體,證明該物質一定是碳酸鹽 | |
| C. | 點燃氫氣前需要檢驗純度,所以點燃甲烷前也需要檢驗純度 | |
| D. | 向碳酸鈉溶液中滴加無色酚酞溶液,溶液變成紅色,說明碳酸鈉屬于堿類 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com