
【題目】金屬在日常生活中有著廣泛的用途。
(1)下列金屬制品中,利用金屬導熱性的是_________(填字母編號)。
A 金屬硬幣 B 鋁制導線 C 銅制火鍋
(2)煉鐵的原理是一氧化碳與氧化鐵在高溫條件下反應生成鐵和二氧化碳,寫出該反應的化學反應方程式___________。
(3)小米品牌汽車,就是一款擁有自主知識產權的純電動車。它所使用的電池為高鐵電池其原理為高鐵酸鉀(![]() )和單質鋅作用,在釋放出電能的同時生成
)和單質鋅作用,在釋放出電能的同時生成![]() 、氧化鐵及氧化鋅,則反應的化學方程式為__________;反應后鐵元素的化合價變為_________價。
、氧化鐵及氧化鋅,則反應的化學方程式為__________;反應后鐵元素的化合價變為_________價。
(4)等質量的甲、乙、丙三種金屬粉末,與足量的稀硫酸反應(反應后甲、乙、丙三種金屬均顯+2價),生成![]() 的質量與反應時間的關系如下圖所示,下列說法不正確的是_________(填字母編號)。
的質量與反應時間的關系如下圖所示,下列說法不正確的是_________(填字母編號)。
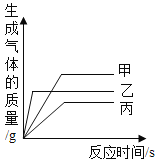
A 三種金屬的活動性:乙>甲>丙 B 生成氫氣的質量:甲>乙>丙
C 相對原子質量:甲>乙>丙 D 消耗硫酸的質量:甲>乙>丙
(5)將一包含有雜質的鐵粉樣品分成質量相等的兩份(樣品中各成分均勻混合:雜質不溶于水,且不參與反應),若向其中一份加入足量的稀鹽酸,充分反應后得到0.4g不溶物;向另一份中加入足量的氯化銅溶液,充分反應后得到不溶物3.6g,則原樣品中鐵粉的質量為_______g。
【答案】C ![]()
![]() +3 C 5.6
+3 C 5.6
【解析】
(1)銅制火鍋利用金屬導熱性;
(2)一氧化碳高溫還原氧化鐵反應原理:3CO+Fe2O3![]() Fe+3CO2;
Fe+3CO2;
(3)高鐵酸鉀與鋅反應原理:2K2FeO4+3Zn=2K2ZnO2+Fe2O3+ZnO;氧化鐵中鐵元素為+3價;
(4)由圖像可知:反應時間越短,金屬越活潑,三種金屬的活動性:乙>甲>丙;生成氫氣的質量:甲>乙>丙;相對原子質量甲<乙<丙;產生的氫氣多消耗硫酸的質量大,甲>乙>丙;
(4)若向其中一份加入足量的稀鹽酸,充分反應后得到0.4g不溶物,則鐵粉中雜質為0.4g,向另一份中加入足量的氯化銅溶液,充分反應后得到不溶物3.6g,則其中包含0.4g雜質,則置換出來銅的質量為3.6g-0.4g=3.2g,
設:鐵的質量為x。
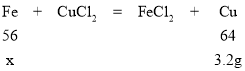
![]() =
=![]() 則x=2.8g
則x=2.8g
鐵粉的質量為2.8g×2=5.6g。


 名校課堂系列答案
名校課堂系列答案科目:初中化學 來源: 題型:
【題目】化學興趣小組在實驗室用含硫酸銅的廢液和氯化鋇溶液反應制取少量氯化銅溶液,并測定該廢液中銅離子的含量。實驗過程和相關數據如下:用燒杯稱取含硫酸銅的廢液120.0 g,滴加氯化鋇溶液至126.6 g時,恰好完全反應,過濾,稱得濾液質量為200.0 g。請計算:(廢液中雜質不參加反應)
(1)反應后生成沉淀的質量是________g;
(2)所得氯化銅溶液中溶質的質量分數________(寫出計算過程);
(3)原硫酸銅溶液中銅離子的質量分數是___________(精確到0.1%)。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】根據下表回答問題。
溫度(C) | 20 | 40 | 50 | 60 | 80 | |
溶解度(g) |
| 36.0 | 36.6 | 37.0 | 37.3 | 38.4 |
| 31.6 | 63.9 | 85.5 | 110 | 169 | |
(1)20℃時,![]() 溶解度是________________g;
溶解度是________________g;
(2)![]() 溶液可以用蒸發溶劑的方法提取溶質的理由是__________;
溶液可以用蒸發溶劑的方法提取溶質的理由是__________;
(3)在60℃時將120g ![]() 和34g
和34g ![]() 溶于100g水中,充分溶解后降溫至20℃,過濾,理論上可得到晶體________________g。
溶于100g水中,充分溶解后降溫至20℃,過濾,理論上可得到晶體________________g。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】實驗室中各種不同儀器,可以組裝成多種不同的裝置,結合下列實驗裝置圖回答問題:

(1)實驗室用石灰石和稀鹽酸反應制取二氧化碳,反應的化學方程式為 ,該反應生成的二氧化碳氣體中常混有少量氯化氫氣體,可通過盛有飽和碳酸氫鈉溶液的G裝置除去氯化氫氣體,請從上圖裝置中選擇并組裝一套制取干燥純凈的二氧化碳的裝置,正確的連接順序為 (用接口處字母填寫).要證明CO2不支持燃燒,密度比空氣大的性質,你認為 (填“H”或“I”)裝置操作效果更好.
(2)實驗室用氯酸鉀和二氧化錳加熱制取氧氣應選擇的制取裝置 (填裝置編號),若用高錳酸鉀為原料制取氧氣,則需要在試管口處放 ,防止堵塞導管,實驗室常用H2O2在二氧化錳催化作用下制取O2,其反應的化學方程式是 .
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】下列實驗方案中,你認為能達到實驗目的的是( )
選項 | 實驗目的 | 實驗方案 |
A | 除去 | 點燃 |
B | 分離 | 加水溶解,過濾,蒸發結晶 |
C | 鑒別合成纖維和羊毛纖維 | 分別取樣灼燒,聞氣味 |
D | 檢驗露置于空氣中的 | 加入過量 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】現有硫酸鎂和硫酸鈉的混合物12.8g,全部溶于50g水中,加入一定質量的氫氧化鈉溶液,恰好完全反應后,過濾,得到5.8g沉淀,所得溶液中溶質的質量分數為15%(不考慮過濾過程中物質質量的損失)。計算:
(1)原混合物中硫酸鈉的質量_______。
(2)所加氫氧化鈉溶液中溶質的質量分數_______(計算結果精確到0.1%)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】中國科學家屠呦呦因青蒿素和雙氫青蒿素而榮獲了諾貝爾獎。興趣小組在老師的指導下對此進行了相關學習與探究。
(資料查閱)(1)青蒿素易溶于乙醚,在水中幾乎不溶。
(2)雙氫青蒿素是由碳、氫、氧元素組成的,且其相對分子質量不大于300。
(實驗探究1)乙醚浸取法制青蒿素的主要工藝如下圖所示:

操作I需要的玻璃儀器主要有:燒杯、漏斗、__________,操作II的原理是利用物質__________的不同。
(實驗探究2)小組同學設計如下圖所示實驗測定雙氫青蒿素的組成,將7.1g的雙氫青蒿素放在燃燒管C中燃燒,回答下列問題。

(1)裝置B中試劑名稱為__________,請將裝置B中的導管補畫完整___________。
(2)寫出E中發生反應的化學方程式______________________。
(3)實驗測得數據如表:
裝置(包括藥品)質量 | 實驗前/g | 實驗后/g |
D | 84.6 | 90.0 |
E | 90.2 | 106.7 |
根據所給數據計算出雙氫青蒿素中的碳元素和氫元素的質量比為___________。
(4)寫出雙氫青蒿素充分燃燒的化學方程式:______________________。
(反思拓展)對“實驗探究2”的分析,下列說法正確的是___________。
A 若缺少裝置B,則測出的雙氫青蒿素中氫元素的質量偏大
B 若缺少氧化銅,則測出的雙氫青蒿素中碳、氧元素的質量比偏小
C 若缺少裝置F,則測出的雙氫青蒿素中碳元素質量偏小。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】蔗糖的化學式![]() ,是食品中常用的甜品劑。請回答下列問題:
,是食品中常用的甜品劑。請回答下列問題:
(1)蔗糖中C、H、O三種元素的原子個數比為_________。
(2)蔗糖中碳元素和氫元素的質量比為________。
(3)要配制15%的蔗糖溶液160g,需要蔗糖的質量是________g。
(4)要把(3)配得的溶液稀釋為5%,需要加水的質量是________g。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】在宏觀、微觀和符號之間建立聯系是化學學科的特點。
(1)物質的組成及構成關系如圖1所示,圖中①表示的是 ,②表示的是 。
(2)下列說法正確的是 (填字母)。
A.氯化氫是由氫、氯兩種元素組成的
B.氯化氫是由氫氣和氯氣混合而成的
C.氯化氫是由一個氫原子和一個氯原子構成的

(3)圖2是氧、硫、氯三種元素的原子結構示意圖。
①氯原子的結構示意圖中x的數值是 。
②氧和硫兩種元素的化學性質具有相似性的原因是它們原子的 相同。
③氧和氯兩種元素最本質的區別是它們原子中的 相同。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com