
分析 根據質量守恒定律計算生成氧氣的質量,然后依據氯酸鉀在二氧化錳的催化作用下生成氯化鉀和氧氣,結合氧氣的質量計算氯化鉀的質量,計算參加反應的氯酸鉀的質量,然后計算未參加反應的氯酸鉀質量.
解答 解:生成氧氣的質量為:60g-40.8g=19.2g,
設生成氯化鉀的質量為y,參加反應的氯酸鉀質量為z
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 149 96
z y 19.2g
$\frac{245}{z}$=$\frac{149}{y}$=$\frac{96}{19.2g}$
y=29.8g
z=49g
所以二氧化錳質量為:60g-49g=11g.
答:反應后的固體物質是氯化鉀和二氧化錳,質量分別是:29.8g,11g.
點評 解答此類題的方法是:首先利用質量守恒定律,根據反應前后固體物質質量差求得反應生成氣體的質量;然后,利用化學方程式由氣體質量計算其他物質的質量.


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:解答題
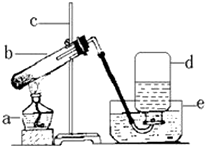 如圖為實驗室用加熱高錳酸鉀的方法制取氧氣的裝置圖,回答問題:
如圖為實驗室用加熱高錳酸鉀的方法制取氧氣的裝置圖,回答問題:查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 鎂--“我是銀白色” | B. | 一氧化碳--“我可燃燒” | ||
| C. | 氫氣--“我是最輕的氣體” | D. | 金剛石--“我是最硬的礦物” |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | ①②⑤⑦⑧ | B. | ①②③⑦ | C. | ⑤⑥⑧ | D. | ①②⑤⑥⑦⑧ |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題

查看答案和解析>>
科目:初中化學 來源: 題型:選擇題

| A. | B試管中產生的氣體的化學式是氫氣 | |
| B. | 電池的正極與試管A中的電極相連 | |
| C. | A管和B管所產生氣體的質量比是2:1 | |
| D. | 水通直流電能分解生成氫氣和氧氣,說明水是由氫、氧兩種元素組成 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com