
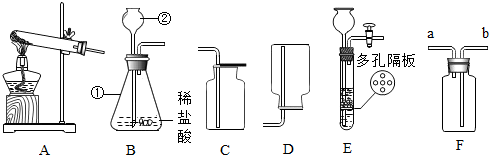
分析 (1)據常用儀器回答;
(2)①根據石灰石和稀鹽酸反應原理書寫方程式;
②根據裝置特點分析其優點;
③洗氣裝置中導管要長進短出,二氧化碳與石灰水的主要成分氫氧化鈣反應生成碳酸鈣沉淀和水,據此分析解答;
(3)用固體氯化銨和固體熟石灰混合加熱制取NH3,屬于固體加熱型,故選發生裝置A,并據反應原理書寫方程式;氨氣溶于水顯堿性,能使紅色石蕊試紙變藍色,據此驗滿,氨氣密度比空氣小,應從短管進氣.
解答 解:(1)標號儀器分別是錐形瓶和長頸漏斗;
(2)①石灰石的主要成分碳酸鈣和鹽酸反應生成氯化鈣、水和二氧化碳,發生反應的化學方程式為:CaCO3+2HCl═CaCl2+H2O+CO2↑;
②若將發生裝置由B改為E,則可通過活塞開閉隨時控制反應的發生和停止;
③在F中加入澄清石灰水可檢驗CO2,應將B裝置的導管與F裝置的導管b連接,讓氣體充分與石灰水接觸,二氧化碳與石灰水的主要成分氫氧化鈣反應生成碳酸鈣沉淀和水,反應的化學方程式為:Ca(OH)2+CO2═CaCO3↓+H2O;
(3)用固體氯化銨和固體熟石灰混合加熱制取NH3,屬于固體加熱型,故選發生裝置A,兩種物質反應屬于復分解反應,相互交換成分生成氯化鈣、水和氨氣,反應方程式是:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;氨氣溶于水顯堿性,能使紅色石蕊試紙變藍色,氨氣密度比空氣小,應從短管進氣,將空氣擠壓到集氣瓶底部排出,所以可將濕潤的紅色石蕊試紙放于b導管處,若變藍則滿;
故答案為:(1)錐形瓶;長頸漏斗;
(2)①CaCO3+2HCl═CaCl2+H2O+CO2↑;②C;③b;Ca(OH)2+CO2═CaCO3↓+H2O;
(3)A;2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;濕潤的紅色;b.
點評 本題考查裝置的選擇、化學方程式的書寫,裝置評價、氣體驗滿等知識,選擇發生裝置時,要考慮反應物的狀態、反應條件等因素;選擇收集裝置時,要考慮氣體的水溶性、密度、能否和空氣中的物質發生化學反應等因素.


 星級口算天天練系列答案
星級口算天天練系列答案 芒果教輔達標測試卷系列答案
芒果教輔達標測試卷系列答案科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 硝酸鉀 食醋 金剛石 | B. | 水銀 白磷 高錳酸鉀 | ||
| C. | 冰水混合物 液氧 干冰 | D. | 鐵銹 銅 水 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
 硝酸鉀、氯化鉀固體的溶解度曲線如圖:
硝酸鉀、氯化鉀固體的溶解度曲線如圖:查看答案和解析>>
科目:初中化學 來源: 題型:填空題
 根據如圖某牙膏商標上的部分文字,用化學用語填空.
根據如圖某牙膏商標上的部分文字,用化學用語填空.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com