
分析 (1)硫酸銅溶于水發生電離;
(2)根據溶液具有均一性,均一性是指溶液中各部分性質相同,據此進行分析解答;
(3)根據化合物中某元素的質量=該化合物的質量×該元素的質量分數,進行分析解答;
(4)利用溶質質量=溶液質量×溶質的質量分數,可得硫酸銅質量,結合化學方程式計算生成白色沉淀的質量.
解答 解:(1)溶液由溶質(硫酸銅)和溶劑(水)組成,硫酸銅是由銅離子和硫酸根離子構成,水由水分子構成,根據離子和分子的書寫為:Cu2+、SO42-、H2O.
(2)因原硫酸銅溶液溶質的質量分數為8%,根據溶液具有均一性可知,則取出的20克與原溶液中溶質質量分數相同,均為8%,
(3)200g8%硫酸銅溶液含溶質硫酸銅的質量為16g,需稱取硫酸銅晶體的質量為8g÷($\frac{160}{250}$×100%)=25g.
(4)20g該硫酸銅溶液中硫酸銅的質量為20g×8%=1.6g
設生成硫酸鋇沉淀質量為x
BaCl2+CuSO4=BaSO4↓+CuCl2
160 233
1.6g x
$\frac{160}{1.6g}=\frac{233}{x}$
x=2.33g
故答案為:(1)Cu2+ SO42- H2O;(2)8%;(3)25;(4)2.33.
點評 本題難度不大,掌握溶質質量分數的有關計算、化學式和化學方程式的有關計算并能靈活運用是正確解答本題的關鍵.


 提分百分百檢測卷單元期末測試卷系列答案
提分百分百檢測卷單元期末測試卷系列答案 小學期末標準試卷系列答案
小學期末標準試卷系列答案科目:初中化學 來源: 題型:選擇題
| A. | 64% | B. | 40% | C. | 36% | D. | 69.5% |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 含有C、H 兩種元素,可能含有O 元素 | |
| B. | 含有C、H 兩種元素,不含O 元素 | |
| C. | 含有C、H、O 三種元素 | |
| D. | 含有C、O 兩種元素,不含H 元素 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
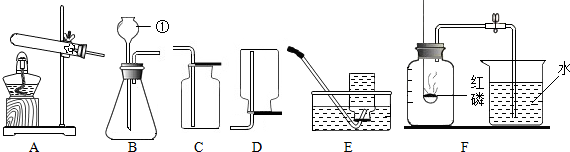
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:多選題
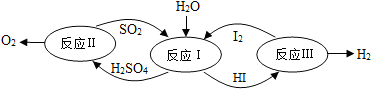 氫能是一種極具發展潛力的清潔能源.以太陽能為熱源,熱化學硫碘循環分解水是一種高效、無污染的制氫方法.其反應過程如圖所示,下列說法正確的是( )
氫能是一種極具發展潛力的清潔能源.以太陽能為熱源,熱化學硫碘循環分解水是一種高效、無污染的制氫方法.其反應過程如圖所示,下列說法正確的是( )| A. | 該流程可實現太陽能向化學能的轉化 | |
| B. | 制得H2中氫元素最初來源于水和硫酸 | |
| C. | 所有涉及的反應中,有三種元素的化合價發生了改變 | |
| D. | 反應I中,發生反應的化學方程式為SO2+I2+2H2O=2HI+H2SO4 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
 某化學反應過程的微觀示意圖如下.下列說法錯誤的是( )
某化學反應過程的微觀示意圖如下.下列說法錯誤的是( )| A. | 原子是化學變化中的最小粒子 | |
| B. | 元素的種類、原子的數目在化學反應前后不變 | |
| C. | 在化學變化中分子分成原子,原子又重新組合成新物質的分子 | |
| D. | 上述反應的化學方程式可表示為:2A2B2=A2B+2B |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | AgNO3→MgCl2 | B. | KNO3→MgCl2 | C. | NaCl→MgCl2 | D. | Mg(OH)2→MgCl2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com