
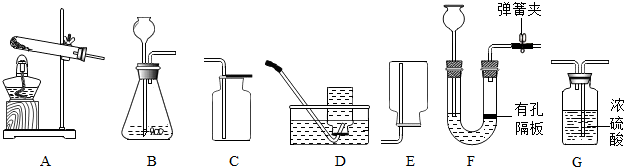
分析 ①根據反應物的狀態和反應條件均可選出氫氣、氧氣、二氧化碳的發生裝置;
②二氧化碳的驗滿是用燃著的木條放在瓶口觀看木條是否熄滅的方法;
③用高錳酸鉀制取氧氣時,試管口應放一團棉花,反應過程中氧原子的利用率可根據化學方程式中氧原子的個數求出,高錳酸鉀完全分解后,要回收二氧化錳,可利用二氧化錳和錳酸鉀的溶解性不同分離混合物;
④蒸發結晶時為防止液滴向四周飛濺,可用玻璃棒攪拌;
解答 解:
(1)用鋅和稀硫酸制氫氣應選擇固液常溫性發生裝置,又氫氣的密度比空氣小且難溶于水,所以發生裝置可選B或F,操作時相對比較方便,能隨開隨用可選用F;收集裝置可選D或E,為收集到較純凈的氫氣應選擇排水法收集.故選F;D.
(3)實驗室用石灰石和稀鹽酸反應生成氯化鈣、水和二氧化碳,但若用碳酸氫鈉加熱制取二氧化碳,化學反應方程式即為:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,發生裝置應選固體加熱型.
故選CaCO3+2HCl=CaCl2+H2O+CO2↑;2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;A;用燃著的木條放置于瓶口,木條熄滅.
(4)用高錳酸鉀制氧氣時,為防止高錳酸鉀粉末進入導管,需在試管口放一團棉花,根據高錳酸鉀分解的化學方程式可以看出參加反應的氧原子8個,生成物中氧氣中氧原子數只有2個,所以氧原子的利用率為2÷8=25%.
故答案為:在試管口放一團膨松的棉花;25%(或1/4).
(5)高錳酸鉀完全分解后剩余物中只有二氧化錳和錳酸鉀,而二氧化錳不溶于水,錳酸鉀溶于水,所以可以利用溶解過濾的方法得到二氧化錳,然后進行洗滌干燥即可,故選②③④①.
(6)蒸發時為防止液滴向四周飛濺,所以要用玻璃棒不停的攪拌,故答案為:攪拌使液體受熱均勻,防止飛濺.
答案:
(1)FD
(2)BGC或FGC 2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ A 用燃著的木條放置于瓶口,木條熄滅則已經滿了.
(3)在試管口放一團膨松的棉花 25%(或1/4)
(4)②③④①
(5)攪拌使液體受熱均勻,防止飛濺
點評 本題綜合考查氣體的實驗室制法原理和裝置選擇,同時進行類比訓練和知識延伸,與混合物的分離聯系起來進行考查.


科目:初中化學 來源: 題型:解答題
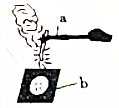 如圖所示是鎂帶燃燒實驗,回答下列問題:
如圖所示是鎂帶燃燒實驗,回答下列問題:查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 某些食品密封包裝時充入氮氣 | B. | 用較濃的食醋除水垢 | ||
| C. | 煤燃燒時向煤爐中不斷地鼓入空氣 | D. | 面團發酵時放在溫熱處 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
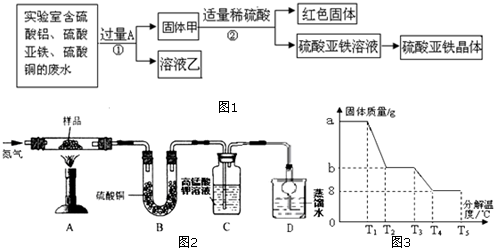
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
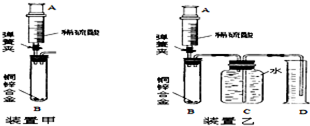 學習小組的同學在老師的幫助下對黃銅中銅和鋅的含量展開探究.
學習小組的同學在老師的幫助下對黃銅中銅和鋅的含量展開探究.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com