
分析 根據質量守恒定律:反應前后各原子的數目不變,選擇相應的配平方法(最小公倍數法、定一法等)進行配平即可;配平時要注意化學計量數必須加在化學式的前面,配平過程中不能改變化學式中的下標;配平后化學計量數必須為整數.
解答 解:①本題可利用“定一法”進行配平,把Fe2O3的化學計量數定為1,則FeS2、O2、SO2前面的化學計量數分別為:2、$\frac{11}{2}$、4,同時擴大2倍,則FeS2、O2、Fe2O3、SO2前面的化學計量數分別為:4、11、2、8.
②本題可利用“定一法”進行配平,把Na2SO4的化學計量數定為1,則CuSO4、NaOH、Cu(OH)2前面的化學計量數分別為:1、2、1.
③本題可利用“定一法”進行配平,把C2H2的化學計量數定為1,則O2、H2O、CO2前面的化學計量數分別為:$\frac{5}{2}$、1、2,同時擴大2倍,則C2H2、O2、CO2、H2O前面的化學計量數分別為2、5、4、2.
故答案為:①4、11、2、8;②1、2、1、1;③2、5、4、2.
點評 本題難度不大,配平時化學計量數必須加在化學式的前面,配平過程中不能改變化學式中的下標;配平后化學計量數必須為整數,配平過程中若出現分數,必須把分數去分母轉化為整數.


 口算心算速算應用題系列答案
口算心算速算應用題系列答案 同步拓展閱讀系列答案
同步拓展閱讀系列答案科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
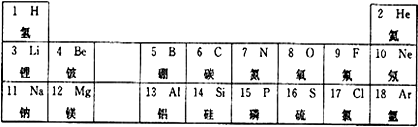
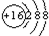 所表示的粒子符號為S2-;
所表示的粒子符號為S2-;查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| 物質 | a | b | c | d |
| 反應前的質量/g | 30 | 20 | 15 | 10 |
| 反應后的質量/g | x | 23 | y | 16 |
| A. | x+y=35 | |
| B. | 發生變化的b與d質量比為1:2 | |
| C. | 當y≥15時,該反應不一定是分解反應 | |
| D. | 當x為25時,y一定為10 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com