

分析 (1)向盛有BaCl2和HCl的混合溶液中滴加Na2CO3溶液時,碳酸鈉先與鹽酸反應產生二氧化碳,當鹽酸反應完后,再與氯化鋇反應產生碳酸鋇沉淀;
(2)開始時是生成氣體的,由于加入的是碳酸鈉溶液,而生成的是二氧化碳氣體,兩者的質量明顯是增加多,減少的少,所以曲線明顯上揚.當不再生成二氧化碳時,就生成碳酸鋇,由于碳酸鋇的質量要多于碳酸鈉的,所以導致溶液的質量增加減緩.從圖中曲線可看出,當滴入碳酸鈉106g時,鹽酸完全反應,據此可根據滴入碳酸鈉質量計算放出氣體質量;
(3)從圖中曲線可看出,開始滴入106克的碳酸鈉與鹽酸反應,106克~212克之間滴入碳酸鈉與氯化鋇反應;即與氯化鋇反應的碳酸鈉質量為212克-106克;
由化學方程式知,碳酸鈉和鹽酸、氯化鋇反應后溶液中溶質均為氯化鈉,可根據化學方程式中參加反應的碳酸鈉質量計算生成的氯化鈉質量和碳酸鋇沉淀質量,再根據質量守恒定律,參加反應的物質總質量等于生成的物質總質量,最后所得不飽和溶液的質量等于l00gBaCl2和HCl的混合溶液,加上滴入的212gNa2CO3溶液,減去生成的氣體和沉淀的質量,即可計算所得不飽和溶液中溶質質量分數.
解答 解:(1)碳酸鈉和鹽酸反應產生二氧化碳,有氣體放出,與氯化鋇反應產生碳酸鋇,即有白色沉淀產生;
(2)設實驗過程中放出的氣體總質量為x,則
Na2CO3 ~CO2
106 44
106g×10% x
$\frac{106}{106g×10%}=\frac{44}{x}$
x=4.4g
(3)設實驗過程中產生氯化鈉質量為y,產生碳酸鋇質量為z,則
本關系是指整個過程的,不考慮是碳酸鈉與鹽酸還是和氯化鋇反應,最終對應的鈉都在氯化鈉中.
Na2CO3 ~2NaCl
106 117
212g×10% y
$\frac{106}{212g×10%}=\frac{117}{y}$
y=23.4g
后期的碳酸鈉中碳酸根轉化為碳酸鋇沉淀,所以對應的碳酸鈉是106g溶液之后的部分.
Na2CO3 ~BaCO3
106 197
(212g-106g)×10% z
=106g×10%
$\frac{106}{106g×10%}=\frac{197}{z}$
z=19.7g
所得NaCl溶液的質量分數為:$\frac{23.4g}{100g+212g-19.7g-4.4g}$×100%=8.1%
答案:
(1)有白色沉淀生成;
(2)4.4克
(3)所得不飽和溶液中溶質質量分數是8.1%.
點評 本題考查根據圖象的有關化學方程式的計算,重在考查學生的識圖,碳酸鈉與兩種物質都能發生反應,而首先是與鹽酸反應,其次與氯化鋇反應.(3)小題結合化學方程式考查溶質質量分數的計算,注意在計算溶液總質量是要靈活運用質量守恒定律,最后所得不飽和溶液的質量等于l00gBaCl2和HCl的混合溶液,加上滴入的212gNa2CO3溶液,減去生成的氣體和沉淀的質量,不能多加或少減,此小題較難,學生容易出錯,平時要多注意訓練.(3)小題在計算氯化鈉質量時還可根據鈉元素質量守恒,碳酸鈉中鈉元素全部轉移到氯化鈉中,據此可求出產生氯化鈉質量.


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:選擇題
| A. | YO | B. | YO2 | C. | Y2O3 | D. | Y3O2 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:推斷題
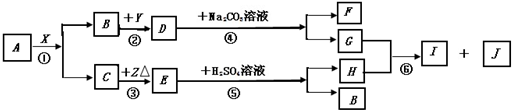
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
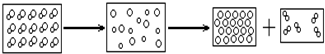
| A. | 氧化汞受熱時能分解成汞和氧氣 | |
| B. | 原子是化學變化中的最小粒子 | |
| C. | 原子是不能再分的粒子 | |
| D. | 化學反應的實質是分子的再分和原子的重新組合 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
 向一定質量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液質量與加入Zn的質量關系如圖所示.下列說法正確的是( )
向一定質量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液質量與加入Zn的質量關系如圖所示.下列說法正確的是( )| A. | 取a點溶液,滴加稀鹽酸,無白色沉淀 | |
| B. | c點溶液中溶質為Zn(NO3)2 | |
| C. | 若取b~c段固體,滴加稀鹽酸,有氣泡產生 | |
| D. | 取d點的固體有2種 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
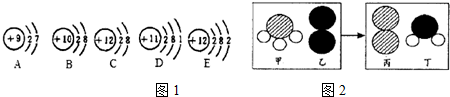
| 抗胃酸藥 | 復方氫氧化鎂片劑 | 鋁碳酸鎂片 |
| 有效成分 | Mg (OH)2 | AlMg(OH)3CO3 |
| 構成微粒 | Mg2+、OH- | A13+、Mg2+、OH-、CO32- |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 氧化物:氧化鐵、生石灰和水 | |
| B. | 復合肥:硝酸銨、磷酸氫二銨、硝酸鉀 | |
| C. | 單質:金剛石、液氧和銅粉 | |
| D. | 合成材料:合成纖維、塑料和合成橡膠 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com