
| 溫度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
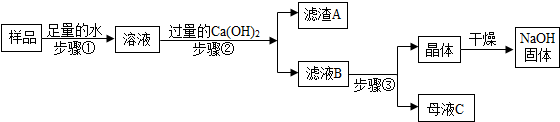
分析 (1)根據表中數據可以獲得的信息是:同溫下氫氧化鈉的溶解度遠遠大于氫氧化鈣的溶解度進行解答;
(2)根據氫氧化鈉的溶解度隨溫度的降低而減小、氧化鈣和水反應放熱,氫氧化鈣的溶解度隨溫度的升高而增大進行解答;
(3)根據變質的氫氧化鈉常會含有碳酸鈉,碳酸鈉與氫氧化鈣反應會生成碳酸鈣與氫氧化鈉,過量的氫氧化鈣會把碳酸鈉清除的更干凈一些.由氫氧化鈉和氫氧化鈣的溶解度與溫度的關系可確定分離它們的方式.
解答 解:(1)根據表中數據可以獲得的信息是:同溫下氫氧化鈉的溶解度遠遠大于氫氧化鈣的溶解度;故填:同溫下氫氧化鈉的溶解度遠遠大于氫氧化鈣的溶解度;
(2)氫氧化鈉的溶解度隨溫度的降低而減小,所以把80℃時NaOH的飽和溶液降溫至20℃,可以看到的現象是:溶液變渾濁;氧化鈣和水反應放熱,氫氧化鈣的溶解度隨溫度的升高而增大,所以現有20℃時Ca(OH)2的飽和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此時溶液的溶質質量分數乙小于甲;故填:溶液變渾濁;<;
(3)(Ⅰ)碳酸鈉和氫氧化鈣反應的化學方程式為:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,加入過量Ca(OH)2的目的是使碳酸鈉完全反應.
故填:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;使碳酸鈉完全反應.
(Ⅱ)步驟③所包含的具體操作是加熱濃縮、降溫結晶、過濾.
故填:降溫結晶.
點評 了解Ca(OH)2、NaOH溶解度的溶解度隨溫度的變化情況,并能據所學知識正確分析解答,本題重在考查對知識的掌握和應用.


科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
| 甲 | 乙 | 丙 | |
| 加入氫氧化鈉溶液質量 (g) | 35.0 | 40.0 | 45.0 |
| 反應得到沉淀的質量 (g) | 2.5 | 2.9 | 2.9 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| 選項 | 實驗目的 | 所用試劑或方法 |
| A | 檢驗NH4NO3溶液和K2SO4溶液 | NaOH溶液或Ba(NO3)2溶液 |
| B | 除去生石灰中含有雜質石灰石 | 水或稀鹽酸 |
| C | 從H2O2溶液制氧氣的殘余物中分離出MnO2 | 過濾或蒸發 |
| D | 區分失去標簽的濃硫酸和稀硫酸 | 水或小木條 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
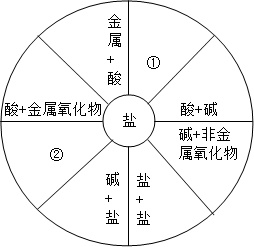 小梅同學學習了單質、氧化物、酸、堿、鹽的性質后,發現許多不同類別的物質反應時能生產鹽,于是她構建了如圖所示的知識網絡圖.借助網絡圖回答:
小梅同學學習了單質、氧化物、酸、堿、鹽的性質后,發現許多不同類別的物質反應時能生產鹽,于是她構建了如圖所示的知識網絡圖.借助網絡圖回答:查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
 環境和食品安全衛生管理,關系百姓身體健康,也是重要的社會民生問題.
環境和食品安全衛生管理,關系百姓身體健康,也是重要的社會民生問題.查看答案和解析>>
科目:初中化學 來源: 題型:解答題
| NaHCO3 | Na2CO3 | |
| 加人稀鹽酸 | 現象Ⅰ | 產生氣泡 |
| 加人飽和石灰水 | 溶液變渾濁 | 現象Ⅱ |
| 加人CaCl2溶液 | 無明顯現象 | 溶液變渾濁 |
| 加熱溶液至沸騰,將氣體通入澄清石灰水 | 澄清石灰水變渾濁 | 澄清石灰水無明顯變化 |
| 實驗步驟 | 實驗現象 | |
| ①取少量樣品溶于水,加人過量 的CaCl2溶液. | 有白色沉淀產生 | 該反應的方程式:Na2CO3+CaCl2═CaCO3↓+2NaCl |
| ②將上述反應后的混合液過濾,取濾液. | 有氣泡冒出 | 證明猜想②成立. |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com