
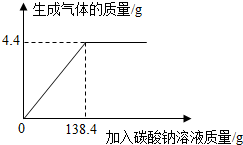
 向一定質量、一定溶質質量分數的稀鹽酸中逐滴加入某碳酸鈉溶液.實驗過程中,產生氣體質量與加入碳酸鈉溶液的質量關系如圖所示,試計算:
向一定質量、一定溶質質量分數的稀鹽酸中逐滴加入某碳酸鈉溶液.實驗過程中,產生氣體質量與加入碳酸鈉溶液的質量關系如圖所示,試計算:分析 (1)由圖中數據可知恰好完全反應時生成CO2的質量;
(2)根據二氧化碳的質量,利用反應的化學方程式計算碳酸鈉的質量,進一步可以計算兩種物質恰好完全反應時所得溶液的溶質質量分數.
解答 解:
(1)恰好完全反應時生成CO2的質量為4.4g;
(2)設恰好完全反應時,所加碳酸鈉溶液中Na2CO3的質量為x,碳酸鈉完全反應生成氯化鈉的質量為y,消耗稀鹽酸的溶質質量為z
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
x z y 4.4g
$\frac{106}{x}=\frac{44}{4.4g}$
x=10.6g
$\frac{73}{z}=\frac{117}{y}=\frac{44}{4.4g}$
z=7.3g
y=11.7g
若恰好完全反應時所得溶液的質量=$\frac{11.7g}{5%}$=234g
稀鹽酸的溶液質量=234g+4.4g-138.4g=100g
則稀鹽酸的溶質質量分數是$\frac{7.3g}{100g}×$100%=7.3%
答案:
(1)4.4;
(2)恰好完全反應時,所加碳酸鈉溶液中Na2CO3的質量是10.6g
(3)稀鹽酸的溶質質量分數是7.3%.
點評 本題主要考查化學方程式進行計算和推斷的能力,計算時要注意規范性和準確性.本題較復雜,計算的知識點多,學生利用圖象分析出二氧化碳的質量代入化學反應方程式計算是解答的突破口.


 閱讀快車系列答案
閱讀快車系列答案科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
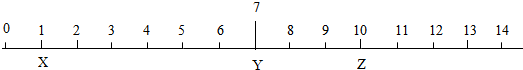
| A. | X顯酸性 | B. | Y一定是水 | ||
| C. | Z可能是碳酸鈉溶液 | D. | Z可使紫色石蕊試液變藍 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
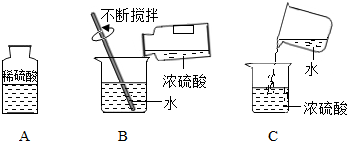
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com