
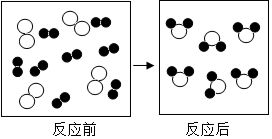
 質量守恒定律的定量研究對化學科學發展具有重大意義.
質量守恒定律的定量研究對化學科學發展具有重大意義. ”分別表示不同的原子).
”分別表示不同的原子). ”微粒.
”微粒.| 物質 | A | B | C | D |  |
| 微觀示意圖 |  |  |  | ||
| 反應前質量/g | 100 | 1 | 1 | 46 | |
| 反應后質量/g | 4 | 55 | 89 | x |
分析 (1)①根據質量守恒定律反應前后原子的種類及數目不變分析;
②根據反應的微觀示意圖中微粒的變化分析化學變化的實質;
(2)①根據質量守恒定律,由物質質量的增減量可確定反應物和生成物的質量,從而得出X的值;
②根據物質中元素的質量可確定構成物質的原子個數比,從而得到物質的化學式,根據化學方程式的書寫步驟可寫出該反應的化學方程式.
解答 解:(1)①由質量守恒定律反應前后原子的種類及數目不變可知,反應后方框內應生成8個 微粒,現已有了6個,應再添加2個
微粒,現已有了6個,應再添加2個 .
.
②由反應的微觀示意圖中微粒的變化可知化學變化的實質是:反應物的原子再重新組合成新物質的分子過程;
(2)①由質量守恒定律及由表中數據可知:二氧化碳的質量增加了89g-1g=88g,可確定二氧化碳是生成物;水蒸氣的質量增加了55g-1g=54g,可確定水蒸氣是生成物;氧氣的質量減少了100g-4g=96g<88g+54g,可確定氧氣和D都是反應物.D減少的質量為:88g+54g-96g=46g,因此X的值為:46-46=0.
②因反應物中的氧氣里只含氧元素,因此生成物中的碳元素和氫元素一定來自D,即D中一定含有碳、氫兩元素,生成物中氧元素的質量為88g×$\frac{16×2}{44}$+54g×$\frac{16}{18}$=112g>96g,可確定生成物中的一部分氧元素來自D,即D中一定含有氧元素,D中碳、氫、氧三元素的原子個數比為:$\frac{88g×\frac{12}{44}}{12}$:$\frac{54g×\frac{1×2}{18}}{1}$:$\frac{112g-96g}{16g}$=2:6:1,故D的化學式為C2H6O,該反應的化學方程式為:C2H6O+3O2$\frac{\underline{\;點燃\;}}{\;}$2CO2+3H2O.
故答為:(1)①2,②反應物的原子再重新組合成新物質的分子過程;(3)0,C2H6O+3O2$\frac{\underline{\;點燃\;}}{\;}$2CO2+3H2O.
點評 此題是對化學反應的微觀過程的考查,解題的關鍵是依據已有的化學反應實質和結合圖示物質的結構進行.


科目:初中化學 來源: 題型:解答題



查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 物質都是由元素組成的 | |
| B. | 原子序數等于該元素原子核內的質子數 | |
| C. | 元素既論種又論個 | |
| D. | 在化學變化中元素的種類不發生改變 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 在點燃條件下,質量比為1:1的硫和氧氣恰好完全化合成二氧化硫 | |
| B. | 在點燃條件下,質量比為1:2的碳和氧氣恰好完全化合成二氧化碳 | |
| C. | 在點燃條件下,分子個數比為2:1的氫氣和氧氣恰好完全化合成水 | |
| D. | 在反應3Fe+2O2$\frac{\underline{\;點燃\;}}{\;}$Fe3O4中,Fe、O2、Fe3O4三種物質的質量比為168:64:232 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題

查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
 “微粒運動實驗”再探究.
“微粒運動實驗”再探究.查看答案和解析>>
科目:初中化學 來源: 題型:計算題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com