
分析 根據硫酸與氯化鋇反應的化學方程式由沉淀的質量可以計算出廢水中硫酸的質量;由于廢水中除含硫酸外還含有鹽酸,也能中和氫氧化鉀,使消耗的氫氧化鉀會增大,再由消耗的氫氧化鉀的質量計算出的硫酸的質量會比廢水中硫酸的質量大.
解答 解:
(1)根據硫酸與氯化鋇反應生成硫酸鋇沉淀,反應過程中觀察到的明顯實驗現象是出現白色沉淀;
(2)100克10.4%的BaCl2溶液中BaCl2的質量為:100g×10.4%=10.4g;
設生成硫酸鋇沉淀的質量為x.
H2SO4+BaCl2=BaSO4↓+2HCl
208 233
10.4g x
$\frac{208}{10.4g}=\frac{233}{x}$
x=23.3g
反應后所得溶液的質量=50g+100g-23.3g=126.7g
(3)由于廢水中除含硫酸外還含有鹽酸,鹽酸也能中和氫氧化鉀,使消耗的氫氧化鉀會增大,再由消耗的氫氧化鉀的質量計算出的硫酸的質量會比廢水中硫酸的質量大(其實就是因為鹽酸消耗的氫氧化鉀也被當成硫酸消耗的,所以導致硫酸的含量偏高).
故答案為:
(1)出現白色沉淀;
(2)反應后所得溶液的質量為126.7g:
(3)偏高;廢水中含有鹽酸,鹽酸也會消耗氫氧化鉀.
點評 本題考查了酸的化學性質以及根據化學方程式的計算,完成此題,可以根據已有的酸的性質以及根據化學方程式的有關計算進行.


 名校課堂系列答案
名校課堂系列答案科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
 ”和“
”和“ ”分別表示兩種不同原子)( )
”分別表示兩種不同原子)( )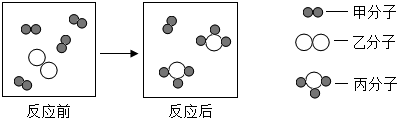
| A. | 該反應前后分子的種類發生了改變 | |
| B. | 該反應前后各種元素的化合價都不變 | |
| C. | 該反應的化學方程式中甲、乙、丙的化學計量數之比是4:1:2 | |
| D. | 反應后分子總數減少,因此物質的總質量也減少 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 用帶火星的木條插入到集氣瓶中檢驗內氧氣是否已滿 | |
| B. | 食鹽水蒸發得到固體食鹽和水蒸氣是分解反應 | |
| C. | 把氯酸鉀和高錳酸鉀混合加熱,比單獨加熱氯酸鉀制出氧氣的速率快 | |
| D. | 因為氧氣比水輕,所以可以用排水法收集 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 表示一個鎂原子 | B. | 只表示一個鎂元素 | ||
| C. | 只是鎂元素和鎂分子 | D. | 既表示鎂元素又表示一個鎂原子 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 20% | B. | 35% | C. | 60% | D. | 80% |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com