

分析 根據原物質和雜質的性質選擇適當的除雜劑和分離方法,所謂除雜(提純),是指除去雜質,同時被提純物質不得改變.除雜質題至少要滿足兩個條件:①加入的試劑只能與雜質反應,不能與原物質反應;②反應后不能引入新的雜質.
解答 解:(1)除去KCl溶液中少量的MgCl2和MgSO4,即除去 鎂離子和硫酸根離子,其離子符號分別是Mg2+、SO42-.
(2)除去鎂離子可用氫氧根離子,除去硫酸根離子可用鋇離子,加碳酸鉀要放在加氫氧化鋇溶液之后,可以將過量的鋇離子沉淀,可顯加入過量的氫氧化鋇溶液,氫氧化鋇與氯化鎂、硫酸鎂反應生成氫氧化鎂沉淀、硫酸鋇沉淀,再加入過量的碳酸鉀溶液,碳酸鉀與過量的氫氧化鋇溶液反應生成碳酸鋇沉淀和氫氧化鉀,碳酸鉀與氯化鋇溶液反應生成碳酸鋇沉淀和氯化鉀;再加入適量的稀鹽酸,除去過量的碳酸鉀溶液和氫氧化鉀溶液;A、B、C三種試劑分別是氫氧化鋇溶液、碳酸鉀溶液、稀鹽酸.
(3)加入過量A后,過濾出的沉淀有硫酸鋇和氫氧化鎂.
(4)在加入A后所得的濾液里加入過量B,即碳酸鉀與過量的氫氧化鋇溶液反應生成碳酸鋇沉淀和氫氧化鉀,碳酸鉀與氯化鋇溶液反應生成碳酸鋇沉淀和氯化鉀,反應的化學方程式為:Ba(OH)2+K2CO3═BaCO3↓+2KOH、BaCl2+K2CO3═BaCO3↓+2KCl.
(5)在加入B后所得的濾液里還要加入適量的C,其目的是除去過量的碳酸鉀和生成的氫氧化鉀.
故答案為:(1)Mg2+、SO42-;(2)⑤④②;(3)硫酸鋇和氫氧化鎂;(4)Ba(OH)2+K2CO3═BaCO3↓+2KOH;BaCl2+K2CO3═BaCO3↓+2KCl;(5)除去過量的碳酸鉀和生成的氫氧化鉀.
點評 物質的分離與除雜是中考的重點,也是難點,解決除雜問題時,抓住除雜質的必需條件(加入的試劑只與雜質反應,反應后不能引入新的雜質)是正確解題的關鍵.


 名校課堂系列答案
名校課堂系列答案科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 一定沒有發生化學變化 | B. | 一定發生了化學變化 | ||
| C. | 有可能發生了化學變化 | D. | 無法推斷 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 兩者都不會改變 | B. | 前者會變小,后者會變大 | ||
| C. | 兩者都會變小 | D. | 前者變大,后者會變小 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. |  測定空氣中氧氣的含量 | B. |  加熱后、聞氣體的氣味 | ||
| C. | 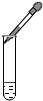 向試管中滴加液體 | D. | 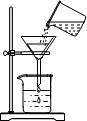 過濾 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
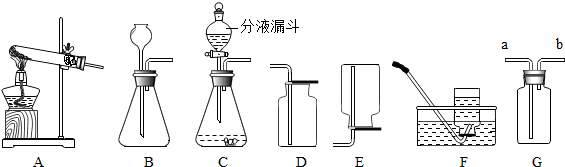
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com