
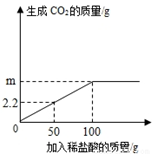
 為了測定某石灰石中碳酸鈣的質量分數,準確稱取12.5g石灰石樣品,研碎后放入燒杯中,向其中加入足量稀鹽酸,(雜質不與鹽酸反應,也不溶于水),實驗測得的數據如圖所示.
為了測定某石灰石中碳酸鈣的質量分數,準確稱取12.5g石灰石樣品,研碎后放入燒杯中,向其中加入足量稀鹽酸,(雜質不與鹽酸反應,也不溶于水),實驗測得的數據如圖所示. 分析 (1)依據粉碎后物質間的接觸更充分從而能促進反應物反應的更徹底分析解答;
(2)根據反應的鹽酸的質量關系判斷生成二氧化碳的質量即可;
(3)利用二氧化碳的質量結合反應的方程式求出碳酸鈣的質量,即可求出石灰石樣品中碳酸鈣的質量分數.
解答 解:(1)由于石灰石樣品研碎后碳酸鈣和鹽酸的接觸面積變大,從而可以使碳酸鈣反應完全;
(2)由圖象可知50g鹽酸可以生辰2.2g二氧化碳,則100g鹽酸反應則會生成二氧化碳4.4g,故m=4.4g;
(3)設碳酸鈣的質量是x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
100
$\frac{100}{44}=\frac{x}{4.4g}$
x=10g
則該石灰石樣品中碳酸鈣的質量分數為$\frac{10g}{12.5g}$×100%=80%;
故答案為:(1)使碳酸鈣反應完全;(2)4.4;(3)該石灰石樣品中碳酸鈣的質量分數為80%.
點評 準確判斷圖中刻度值是正確解決本題一個重要細節,因此正確判斷生成二氧化碳質量是解題的關鍵.


 快捷英語周周練系列答案
快捷英語周周練系列答案科目:初中化學 來源: 題型:解答題
| 實驗步驟 | 設計要求 |
| ①準備兩個大小相同的燒杯,分別標為A、B;向兩燒杯中分別倒入30克粗細相同的食鹽. | 選擇合適的實驗器材 |
| ②向A燒杯倒入20克水,向B燒杯倒入60克水. | 設置對照實驗 |
| ③都用玻璃棒充分攪拌直到A、B兩燒杯底部的食鹽不再溶解為止,過濾、干燥剩余食鹽 | 控制實驗條件 |
| ④稱量并記錄,并進行統計分析. | 觀察和記錄 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
| 實驗步驟 | 實驗現象 | 實驗結論 |
| 1、將白色粉末放于水中. | 白色粉末溶于水,形成無色溶液 | \ |
| 2、將無色酚酞滴入步驟1形成的無色溶液中. | 溶液顏色變紅 | 該溶液呈堿性 |
| 3、在步驟2所形成的溶液中加入稀鹽酸.并在試管口放一根燃燒的火柴. | 溶液由紅色變成無色,燃燒的火柴熄滅了. | 溶液中含有碳酸根離子.白色粉末中含有氫氧化鈉變質后生成的碳酸鈉 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
| 溫度/℃ | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | 氯化鈉 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| 硝酸鉀 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
 (1)構建知識網絡是化學學習中重要的學習方法,小玲同學利用左手構建酸的性質知識網絡,如圖所示,請結合圖示回答下列問題:
(1)構建知識網絡是化學學習中重要的學習方法,小玲同學利用左手構建酸的性質知識網絡,如圖所示,請結合圖示回答下列問題:查看答案和解析>>
科目:初中化學 來源: 題型:填空題
| 實驗操作 | 實驗現象 | 實驗結論 |
| 該氣體是二氧化碳 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
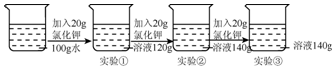
| A. | 該溫度下氯化鉀的溶解度是60g | |
| B. | 實驗②所得溶液中溶質的質量分數為40% | |
| C. | 實驗②和實驗③所得溶液的濃度相同 | |
| D. | 實驗①、②、③的溶液都是飽和溶液 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 某無色溶液中滴加無色酚酞試劑顯紅色,該溶液一定是堿的水溶液 | |
| B. | 某溶液中滴加BaCl2,產生不溶于稀硝酸的白色沉淀,該溶液中一定含有SO42- | |
| C. | 驗證某溶液中是否含有Cl-,先加AgNO3溶液,再加稀硝酸,若有白色沉淀生成,則證明該溶液中有Cl- | |
| D. | 某固體中加入稀鹽酸,產生無色無味的氣體,該固體中不一定含有CO32- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com