
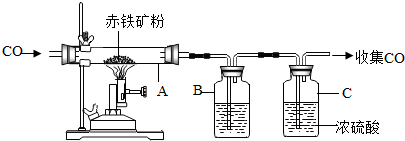
分析 (1)根據物質的用途與性質來分析;
(2)根據氧化鐵反應后生成鐵的顏色變化分析,依據反應的事實結合反應方程式書寫的原則方程式的書寫,根據反應生成二氧化碳考慮氣體的除雜問題;
(3)根據已有的生鐵和鋼的知識進行分析解答即可;
(4)根據四種金屬活動性強弱關系:鋅>鐵>H>銅>銀,在硝酸銀和硝酸銅、硝酸鋅的混合溶液中,加入一定量的鐵粉,鐵能與硝酸銀、硝酸銅依次發生反應.將固體與液體分離使用過濾的方法.
解答 解:(1)鋁可以制成鋁箔,這是利用了金屬的延展性;故填:延展性;
(2)實驗室煉鐵,A中發生反應是,一氧化碳把三氧化二鐵還原為鐵,并生成二氧化碳氣體,現象是:紅色固體變黑色;化學反應方程式是:3CO+Fe2O3 $\frac{\underline{\;高溫\;}}{\;}$2Fe+3CO2;收集較純凈的一氧化碳要除去反應生成的二氧化碳和水蒸氣,把氣體通入盛放氫氧化鈉溶液的試劑瓶,除去二氧化碳,再通入濃硫酸干燥氣體;故填:紅色固體變黑色;3CO+Fe2O3 $\frac{\underline{\;高溫\;}}{\;}$2Fe+3CO2;氫氧化鈉(或NaOH);
(3)生鐵和鋼都是鐵的合金.它們性能存在差異的主要原因是由于其含碳量不同,故填:碳;含碳量;
(4)在硝酸銀和硝酸銅的混合溶液中,加入一定量的鐵粉,鐵能與硝酸銀、硝酸銅依次發生反應,因此一定會發生的反應是鐵和硝酸銀反應產生硝酸亞鐵和銀,鐵與硝酸銅反應生成銅和硝酸亞鐵;將鐵粉、銅粉和銀粉的混合物分離可加入過量的稀鹽酸,鐵粉充分反應,而銀粉和銅粉與之不反應,然后過濾即可.
故填:Fe+2AgNO3=Fe(NO3)2+2Ag;Fe+Cu(NO3)2═Fe+Cu(NO3)2;過量的稀鹽酸;過濾;Fe+2HCl=FeCl2+H2↑.
點評 本題主要考查了對金屬活動性順序的靈活應用,只有活動性強的金屬可以把活動性弱的金屬從鹽溶液中置換出來,培養學生分析問題、解決問題的能力.


 導學與測試系列答案
導學與測試系列答案 新非凡教輔沖刺100分系列答案
新非凡教輔沖刺100分系列答案科目:初中化學 來源: 題型:選擇題
| A. | 過氧乙酸分子是由碳、氫、氧三種元素組成的 | |
| B. | 過氧乙酸分子中含有氧氣分子 | |
| C. | 一個過氧乙酸分子是由二個碳原子、三個氧原子、四個氫原子構成 | |
| D. | 過氧乙酸相對分子質量計算式是12+1+12+16+16+16+1 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
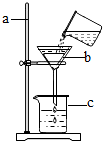 如圖是某同學用來除去水中難溶性雜質時所采用的過濾裝置圖.試回答:
如圖是某同學用來除去水中難溶性雜質時所采用的過濾裝置圖.試回答:查看答案和解析>>
科目:初中化學 來源: 題型:解答題

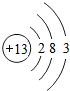 .
.查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 用水檢驗無水硫酸銅、碳酸氫鈉和硫酸鋇粉末 | |
| B. | 不用外加試劑檢驗氯化鐵溶液,氫氧化鈉溶液和氯化鈉溶液 | |
| C. | 用硫酸鈉溶液區分稀鹽酸、氯化鈣溶液和稀硝酸 | |
| D. | 用紫色石蕊溶液區分氫氧化鈉溶液、氯化鈉溶液和鹽酸 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
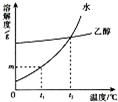 乙醇是一種環境友好的有機溶劑.
乙醇是一種環境友好的有機溶劑.查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com