
| A. | 28% | B. | 42% | C. | 54% | D. | 64% |
分析 設反應后該混合氣體的質量為100g.則混合氣體中含碳元素12g,假設甲烷燃燒完全生成二氧化碳和水,求出此時氮氣的質量,假設甲烷燃燒完全生成一氧化碳和水,求出此時氮氣的質量,氮氣的質量應在共同區間內.
解答 解:
設反應后該混合氣體的質量為100g.則混合氣體中含碳元素12g,則原來甲烷的質量就為12g÷$\frac{12}{16}$=16g,甲烷中氫元素的質量為16g-12g=4g,所以生成水的質量為4g÷$\frac{2}{18}$=36g;所以反應前混合氣的質量為100g+36g=136g.
第一種情況:假設甲烷燃燒完全生成二氧化碳和水:
則二氧化碳的質量為12g÷$\frac{12}{44}$=44g,此時假設氧氣完全反應,剩余的都是氮氣,則氮氣的質量為100g-44g=56g,這樣氮氣的在反應前的混合物中最大質量分數為$\frac{56g}{136g}$×100%=41.2%.而如果剩余氣體中只有氧氣,則氮氣的質量分數為0,所以氮氣的質量分數介于0~41.2%之間.
第二種情況:假設甲烷燃燒完全生成一氧化碳和水:
則一氧化碳的質量為12g÷$\frac{12}{28}$=28g,此時假設氧氣完全反應,剩余的都是氮氣,則氮氣的質量為100g-28g=72g這樣氮氣的在反應前的混合物中最大質量分數為$\frac{72g}{136g}$×100%=52.9%.而如果剩余氣體中只有氧氣,則氮氣的質量分數為0,所以氮氣的質量分數介于0~52.9%.
由于CH4全部轉化為CO、CO2和H2O,也就是同時又二氧化碳和一氧化碳,則反應前的氮氣的質量分數應該是在0~41.2%之間.
故選A.
點評 本題是一道考查混合物質中根據某元素的質量分數來求的另外幾種物質或者元素的質量分數,方法有多種,但可以用排除法做類似的題目;難度較大,培養學生的創新和逆向思維能力.


 通城學典默寫能手系列答案
通城學典默寫能手系列答案科目:初中化學 來源: 題型:實驗探究題
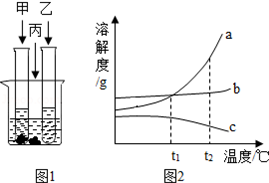
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
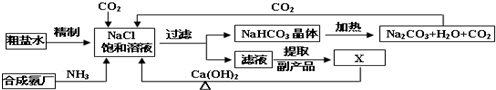
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 提取青蒿素不宜在高溫下進行 | |
| B. | 青蒿素是由碳、氫、氧三種元素組成的 | |
| C. | 青蒿素是由C15H22O5分子構成的 | |
| D. | 青蒿素中碳、氫、氧三種元素的質量比為15:22:5 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
 實驗Ⅰ:實驗室制O2.
實驗Ⅰ:實驗室制O2.查看答案和解析>>
科目:初中化學 來源: 題型:解答題
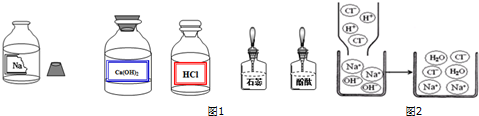
查看答案和解析>>
科目:初中化學 來源: 題型:填空題

查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com