

分析 過氧化氫在二氧化錳催化作用下分解生成水和氧氣,反應前后的質量差即為反應生成氧氣的質量,根據氧氣的質量可以計算過氧化氫的質量,進一步可以計算該過氧化氫溶液中溶質的質量分數.
解答 解:(1)根據質量守恒定律,反應生成氧氣的質量為:34.0g+0.5g-33.7g=0.8g,
故填:0.8g.
(2)二氧化錳在反應過程中起催化作用.
故填:催化.
(3)設過氧化氫質量為x,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
68 32
x 0.8g
$\frac{68}{x}$=$\frac{32}{0.8g}$,
x=1.7g,
該過氧化氫溶液中溶質的質量分數為:$\frac{1.7g}{34.0g}$×100%=5%,
答:該過氧化氫溶液中溶質的質量分數為5%.
點評 差量法在計算中的應用很廣泛,解答的關鍵是要分析出物質的質量差與要求的未知數之間的關系,再根據具體的數據求解.


科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. |  | B. |  | C. | 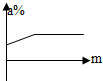 | D. |  |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 甲醛是一種酸 | |
| B. | 甲醛是由氫元素、氧元素和碳元素組成的一種氧化物 | |
| C. | 甲醛有揮發性 | |
| D. | 甲醛分子中碳、氫、氧各原子的個數比為1:1:2 |
查看答案和解析>>
科目:初中化學 來源: 題型:多選題
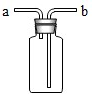
| A. | 收集氫氣時應從b口進入,瓶內空氣從a口排出 | |
| B. | 收集二氧化碳時應從a口進入,瓶內空氣從b口排出 | |
| C. | 當被收集的氣體從a口進入時,瓶內空氣從b口排出,相當于向上排出空氣法收集氣體 | |
| D. | 當被收集的氣體從b口進入時,瓶內空氣從a口排出,相當于向上排出空氣法收集氣體 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com