
【題目】為測定某地石灰石樣品中碳酸鈣的質量分數,進行了以下實驗;向裝有l0.0g石灰石樣品的燒杯中,加入47.2g稀鹽酸,恰好完全反應,燒杯中剩余物質的總質量隨時間變化關系如下表:(石灰石中的雜質不參加反應且難溶于水)

求:(1)最終生成二氧化碳的質量為 g:
(2)樣品中碳酸鈣的質量分數。
【答案】(1)2.2;(2)樣品中CaCO3的質量分數為50%;
【解析】(1)由于石灰石樣品中的碳酸鈣能與稀鹽酸反應,生成氯化鈣、水和二氧化碳(逸出),故反應后燒杯中剩余物質的總質量會減小,根據質量守恒定律可知,減少的質量即為生成的二氧化碳的質量,結合實驗數據可知,燒杯中最終剩余物質的總質量是55.0g,所以生成的二氧化碳質量是10g+47.2g- 55.0g=2.2g。
(2)依據二氧化碳的質量,結合反應的化學方程式,可計算出樣品中碳酸鈣的質量,進而可求出樣品中碳酸鈣的質量分數。
解:設樣品中CaCO3的質量為x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 2.2g
![]()
解得:x=5
則樣品中碳酸鈣的質量分數為![]() ;
;
答:樣品中碳酸鈣的質量分數為50%。
試題分析:根據表格中的數據計算反應前后的質量差即為生成二氧化碳的質量;根據生成二氧化碳的質量,可以計算碳酸鈣的質量,再利用石灰石樣品的質量計算碳酸鈣的質量分數.
考點:根據方程式的相關計算;碳酸鹽與酸的反應原理;質量守恒定律及其應用


科目:初中化學 來源: 題型:
【題目】下列圖像能正確反映其對應關系的是
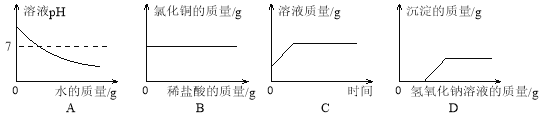
A.向氫氧化鈉溶液中不斷加水,溶液pH與加入水的質量的關系
B.向盛有氧化銅的燒杯中加入稀鹽酸至過量,生成氯化銅質量與加入稀鹽酸質量的關系
C.向一定量的飽和硝酸鉀溶液中加入硝酸鉀固體,溶液的質量與反應時間的關系
D.向鹽酸和硝酸銅的混合溶液中滴加氫氧化鈉溶液,生成沉淀與加入氫氧化鈉溶液的質量關系
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】用來測定空氣成分的方法很多,圖1所示的是小明用紅磷在空氣中燃燒的測定方法。
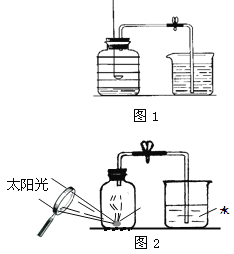
實驗過程是:
第一步:將集氣瓶容積劃分為五等份,并做好標記。
第二步:點燃燃燒匙內的紅磷,伸入集氣瓶中并把塞子塞緊。
第三步:待紅磷熄滅并冷卻后,打開彈簧夾,發現水被吸入極其瓶中,進入集氣瓶中水的體積約為集氣瓶總容積的1/5。
請回答下列問題:
(1)上面的實驗同時證明了氮氣有 的化學性質。
(2)實驗完畢,若進入集氣瓶中水的體積不到總容積的1/5,你認為導致這一結果的原因可能 。
(3)某同學對實驗進行反思后,提出了改進方法(如圖2所示),你認為改進后的優點是: 。
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(8分)某化學興趣小組在室溫的條件下(溫度為20℃),為了測定H2SO4與NaOH發生中和反應時放出的熱量,在左下圖的小燒杯中加入8mL溶質質量分數為10%的NaOH溶液(密度1 g/mL),并滴入3滴酚酞,測量其溫度;另取過量的稀硫酸(密度1.12g/mL),測量其溫度后逐量緩慢地加入到小燒杯中,邊加邊用環形玻璃棒攪拌;測得燒杯中溶液溫度的變化與加入稀硫酸體積之間關系如右下圖所示。

(1)當加入5 mL稀硫酸時,溶液中的溶質有 (填寫溶質化學式)。
(2)當加入約為 mL稀硫酸時,燒杯中溶液的溫度達到最高。此時燒杯中溶液的溫度約為(填寫整數) ℃,燒杯中溶液顏色 。
(3)當加入稀硫酸的體積大于10mL時,溶液溫度下降的原因是 。
(4)當溶液溫度升到最高時,此時溶液中溶質質量分數是多少?(寫出計算過程,共3分)
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】尼古丁的化學式為C10H14N2,下列關于尼古丁的說法正確的是
A.尼古丁由三種元素組成
B.尼古丁是由10個碳原子、14個氫原子、2個氮原子構成
C.尼古丁中氮元素質量分數最大
D.尼古丁中含有氮分子
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】(6分) 用化學用語填空。
(1)2個氮分子______ ; (2)硫酸根離子____;
(3)+2價的鐵元素_______;(4)碳酸鈉_______(5)銅元素___________
(6)天然氣的主要成分的化學式___________
查看答案和解析>>
科目:初中化學 來源: 題型:
【題目】俗話說“真金不怕火煉”最主要是因為( )
A.真金在高溫下不融化
B.真金不用火煉
C.真金遇火不變色
D.金的化學性質不活潑,在高溫下不與氧氣反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com