
 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
| 實驗步驟 | 實驗現象 | 結論 |
| 在少量研碎的水垢中,加入適量的蒸餾水充分攪拌,過濾,在濾液里加入Na2CO3溶液. | 沒有白色沉淀產生 | 沒有氫氧化鈣 |
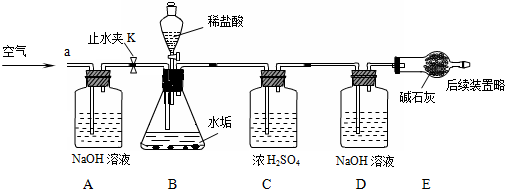
分析 【提出猜想】首先運用題中溶解性表分析得出提出猜想中的兩個空;
【設計方案】實驗1:根據氫氧化鈣溶液能和碳酸鈉反應生成碳酸鈣沉淀進行解答;
【實驗討論】要測定二氧化碳的質量,必須保證裝置氣密性良好;可以根據反應前后裝置D、E的質量差確定生成的二氧化碳的質量,進而確定水垢中是否含有碳酸鎂,計算出所用的鹽酸的質量分數,從而計算求出是否含有氫氧化鎂;
實驗3:根據裝置D的增重判斷生成的二氧化碳的質量為1.25g;
設水垢均為2.50g碳酸鈣,根據方程式計算可生成的二氧化碳1.1g,所以含碳酸鎂;
根據碳酸鈣、碳酸鎂、氫氧化鎂與鹽酸反應的方程式,分別計算它們2.50g消耗鹽酸的質量,其中氫氧化鎂消耗最多,其次為碳酸鎂,假設2.50g全為碳酸鎂,消耗鹽酸56.8g,w>56.8g時,定有氫氧化鎂.
解答 解:【提出猜想】由題中溶解性表知碳酸鈣和氫氧化鎂不溶于水,其余的氫氧化鈣、碳酸鎂微溶,碳酸氫鈣和碳酸氫鎂都溶于水,故水垢的主要成分中一定含有:CaCO3、Mg(OH)2故填:CaCO3;Mg(OH)2;
【設計方案】
實驗1:氫氧化鈣溶液能和碳酸鈉反應生成碳酸鈣沉淀,所以
| 實驗步驟 | 實驗現象 | 結論 |
| 在少量研碎的水垢中,加入適量的蒸餾水充分攪拌,過濾,在濾液里加入Na2CO3溶液. | 沒有白色沉淀產生 | 沒有氫氧化鈣 |
點評 即考查了實驗也考查了根據化學方程式的計算,培養了學生實驗分析能力和根據化學方程式計算能力及運用極值法解題的思想.本題考查了常見物質成分的推斷,完成此題,可以依據物質的性質結合題干提供的信息進行.


科目:初中化學 來源: 題型:解答題

查看答案和解析>>
科目:初中化學 來源: 題型:解答題
| 實驗裝置 |  | 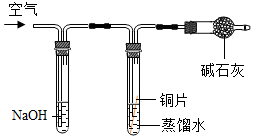 |  | 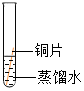 |
| 實驗現象 | 銅片不生銹 | 銅片不生銹 | 銅片不生銹 | 銅片生銹且水面附近銹蝕最嚴重 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題


查看答案和解析>>
科目:初中化學 來源: 題型:解答題
| 實驗步驟 | 實驗現象 |
| 取少量上層料液,滴加稀鹽酸 | 無明顯現象 |
| 另取少量上層料液,滴加碳酸鈉溶液 | 產生白色沉淀 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
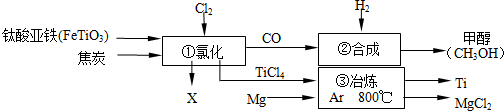
| A. | 鈦酸亞鐵(FeTiO3)中鈦元素為+4價 | |
| B. | ①中反應為:2FeTiO3+6C+7Cl2═2X+2TiCl4+6CO,則X為FeCl3 | |
| C. | ③中氬氣(Ar)作保護氣,反應類型為置換反應 | |
| D. | ②中為使原料全部轉化為甲醇,理論上CO和H2投料的質量比為1:2 |
查看答案和解析>>
科目:初中化學 來源: 題型:填空題
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com