
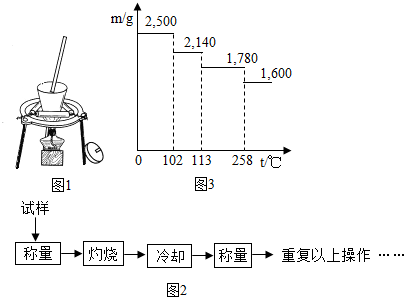
| 加熱前質量 | 加熱后質量 | |
| m1(容器) | m2(容器+晶體) | m(容器+無水硫酸銅) |
| 5.400g | 7.900g | 7.100g |
分析 (1)根據硫酸銅的化學性質來分析;
(2)根據結晶水合物中,結晶水的質量=m(容器十晶體)-m(容器十無水硫酸銅),據化學方程式可以計算結晶水x的值;
(3)在測定中若被測樣品中含有加熱揮發的雜質或實驗前容器中有水,都會造成測量結果偏高、偏低.
(4)根據CuSO4、結晶水物質的量確定化學式.
解答 解:(1)因為硫酸銅能與水發生化學反應,為了防止硫酸銅吸收空氣中的水蒸氣,所以必須在干燥皿中進行冷卻;故填:硫酸銅能和水反應;
(2)由表格中的數據,硫酸銅晶體的質量為7.9g-5.4g=2.5g,水的質量:7.9g-7.1g=0.8g,
則CuSO 4.xH2O$\frac{\underline{\;\;△\;\;}}{\;}$CuSO 4+xH2O,
160+18x 18x
2.5g 0.8g
$\frac{160+18x}{2.5g}=\frac{18x}{0.8g}$
解得x≈4,
故答案為:4;
多次稱量可以減少誤差,至少稱量4次;故填:4;
(3)硫酸銅晶體中,x的值為5,該誤差是水測定結果偏小造成的.
a.硫酸銅晶體中含不可能分解的雜質,會導致測定的硫酸銅的質量偏大,測定的水的質量偏小,符合題意;
b.硫酸銅晶體樣品未加熱完全就開始冷卻,會導致測定的硫酸銅的質量偏大,測定的水的質量偏小,符合題意;
c.加熱過程中有少量晶體濺出,導致水的質量測定結果偏大,不合題意;
d.加熱完畢后,露置在空氣中冷卻,會造成吸水而導致測定的硫酸銅的質量偏大,測定的水的質量偏小,符合題意;
e.實驗前,晶體表面有吸附水,加熱后水揮發,而造成加熱前后固體的質量差偏大,使x值偏大,不合題意.
故填:abd;
(4)2.500g膽礬的物質的量為2.500g÷250g/mol=0.01mol,其中含結晶水的物質的量為0.05mol;102~113℃之間失去結晶水質量為2.500g-2.140g=0.360g,其物質的量為0.360g÷18g/mol=0.02mol;加熱溫度在110℃時,剩余固體中CuSO4與結晶水的物質的量之比為0.01mol:(0.05mol-0.02mol)=1:3,故化學式為CuSO4•3H2O,故填:CuSO4•3H2O.
點評 本題考查了實驗室測定硫酸銅晶體結晶水含量實驗,對失水得到產物的分析判斷以及對實驗結果產生的誤差的原因進行分析是解答的關鍵,題目難度中等.


 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案科目:初中化學 來源: 題型:實驗探究題

查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 往三個集氣瓶中分別倒入少量石灰水并振蕩 | |
| B. | 燃著的木條分別伸入三集氣瓶中 | |
| C. | 用帶火星的木條分別放到三個集氣瓶瓶口 | |
| D. | 以上三種方法都可以 |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | Mg+O2$\frac{\underline{\;點燃\;}}{\;}$MgO2 | B. | S+O2↑$\frac{\underline{\;點燃\;}}{\;}$SO2 | ||
| C. | H2O═H2↑+O2↑ | D. | 2NaOH+CuSO4═Cu(OH)2↓+Na2SO4 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
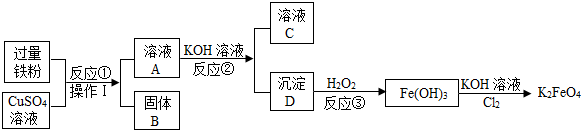
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
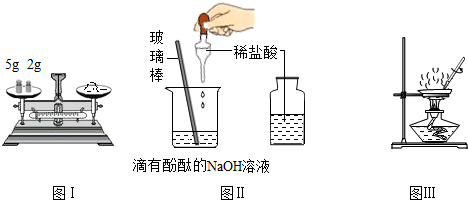
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
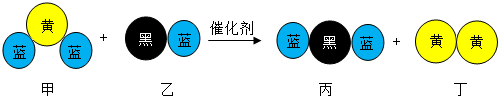
| A. | 乙和丙中所含元素種類相同 | |
| B. | 該反應不可能是置換反應 | |
| C. | 該反應中共有三種元素 | |
| D. | 化學方程式中乙、丁的化學計量數均為1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com