

分析 (1)合金要比組成成分的金屬的硬度大;(2)鐵生銹需要與氧氣和水接觸考慮;(3)在金屬活動性順序中,氫前的金屬能與酸反應生成氫氣,位置在前的金屬能將位于其后的金屬從其鹽溶液中置換出來,利用此知識分析即可;(4)根據題目給出的信息:鐵能夠被磁鐵吸引,因此A是鐵;鎂和銅的混合物中,加入適量的稀硫酸,鎂和硫酸反應生成硫酸鎂和氫氣,銅不反應,因此過濾可以得到B,即金屬銅;(5)根據反應的方程Zn+H2SO4═ZnSO4+H2↑、ZnO+H2SO4═ZnSO4+H2O、找出硫酸與硫酸鋅之間的關系式進行計算.
解答 (1)合金要比組成成分的金屬的硬度大,生鐵片與純鐵片相比,生鐵片硬度大,純鐵硬度小,所以相互刻畫時,在純鐵片表面會留下劃痕.
(2)鐵生銹需要與氧氣和水接觸,所以常在月餅的內包裝袋中放入一小包防腐劑鐵粉,鐵粉的作用是與氧氣發生反應,防止月餅因氧化而變質并且能吸水防潮;
(3)在金屬活動性順序中,鋅>氫>銅>銀,鋅能與硝酸銀反應生成銀和硝酸鋅,可以和硝酸銅反應生成銅和硝酸鋅;所以放入鋅后,鋅要先置換出硝酸銀中銀,再去置換硝酸同種的銅,所以如果向濾渣中加鹽酸有氣泡,則濾渣中一定含有鋅,即加入的鋅過量,所以銀和銅都被置換出來了,所以濾渣中含有銅、鋅、銀;
(4)①鐵能夠被磁鐵吸引,因此A是鐵;鎂和銅的混合物中,加入適量的稀硫酸,鎂和硫酸反應生成硫酸鎂和氫氣,銅不反應,因此過濾可以得到B,即金屬銅;
②硫酸鎂溶液蒸發結晶即可得到硫酸鎂固體;
③步驟②是鎂和硫酸反應生成硫酸鎂和氫氣,其化學方程式為:Mg+H2SO4=MgSO4+H2↑
(5)解:設所得溶液中溶質的質量為x,由Zn+H2SO4═ZnSO4+H2↑、ZnO+H2SO4═ZnSO4+H2O 得:
H2SO4~ZnSO4
98 161
98g×10% x
根據:$\frac{98}{161}=\frac{98g×10%}{x}$解得:x=16.1g
由以上計算可知,A、B、D錯誤,C正確
故答案為:(1)純鐵片
(2)與氧氣發生反應,防止月餅因氧化而變質并且能吸水防潮
(3)Ag、Cu、Zn (4)鐵(或Fe);過濾;Mg+H2SO4=MgSO4+H2↑(5)C.
點評 本考點屬于物質的制備,做本類題型時,要注意題目給出的信息,利用已知條件來解決有關的問題.本題考查了金屬的化學性質,還有酸堿鹽的化學性質,綜合性比較強,要認真掌握.


科目:初中化學 來源: 題型:選擇題
| A. | 制取少量NaOH溶液:將Ca(OH)2溶液和NaCl溶液混合,過濾 | |
| B. | 檢驗NaOH溶液和鹽酸反應后的溶液中是否有鹽酸:取樣,滴加AgNO3溶液 | |
| C. | 分離CaCl2和MgCl2的固體:溶解后,加入適量Ca(OH)2溶液,充分反應后過濾,蒸發 | |
| D. | 驗證Cu的活動性比Ag強:將Ag絲伸入Cu(NO3)2溶液中,觀察表面及溶液顏色是否變化 |
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:多選題
| A. | 樣品中一定沒有CuSO4、CaCl2,一定有NaHCO3 | |
| B. | 樣品中一定含有KNO3,可能含有NaHCO3 | |
| C. | 樣品中一定含有NaHCO3,可能含有KNO3 | |
| D. | 所加的稀硫酸溶質的質量分數不大于9.8% |
查看答案和解析>>
科目:初中化學 來源: 題型:選擇題
| A. | 鎂條在空氣中燃燒發出藍紫色火焰,產生大量白煙 | |
| B. | 電解水正極一側得到的氣體能使帶火星的木條復燃 | |
| C. | 銅絲放入足量稀硫酸中產生大量氣泡,溶液變藍 | |
| D. | 打開濃硫酸的試劑瓶蓋時,瓶口有白霧產生 |
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
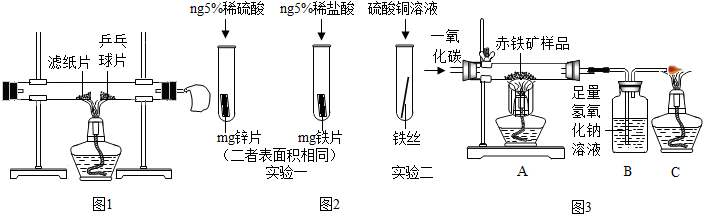
查看答案和解析>>
科目:初中化學 來源: 題型:實驗探究題
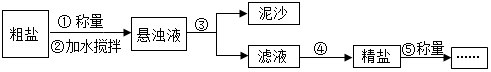
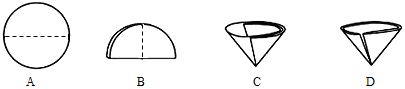
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com