
將一定質量金屬Mg和稀鹽酸恰好完全反應,產生氣體的質量為0.2 g.
(1)反應后溶液中溶質MgCl2的質量為________g.
(2)向反應后的溶液中逐滴加入NaOH溶液,當加入的NaOH溶液質量為20 g時,恰好完全反應,此時,生成沉淀的質量為________g.
(3)計算所加NaOH溶液的溶質質量分數是多少?
答案為:(1)9.5;(2)5.8;(3)40%.
分析:(1)根據化學方程式利用氫氣的質量求出氯化鎂的質量即可;
(2)根據氯化鎂的質量求出氫氧化鎂的質量;
(3)根據氯化鎂的質量求出氫氧化鈉的質量,然后根據溶質質量分數求出氫氧化鈉溶液的溶質質量分數;
解答:解:(1)設反應后溶液中溶質MgCl2的質量為x.
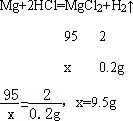
答:反應后溶液中溶質MgCl2的質量為9.5 g.
(2)設所加20 g NaOH溶液中含NaOH的質量為y,生成氫氧化鎂沉淀的質量為z
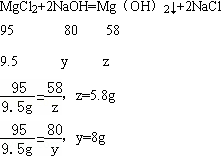
答:生成沉淀的質量為5.8 g.
(3)所加NaOH溶液的溶質質量分數為![]() ×100%=40%.
×100%=40%.
答:所加NaOH溶液的溶質質量分數為40%.
點評:本題難度不是很大,主要考查了根據化學方程式計算有關物質的質量和有關溶質質量分數的計算,培養學生的分析問題、解決問題的能力.
考點:根據化學反應方程式的計算;有關溶質質量分數的簡單計算.


科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源:2012年初中畢業升學考試(四川瀘州卷)化學(解析版) 題型:計算題
(2012•瀘州)將一定質量金屬Mg和稀鹽酸恰好完全反應,產生氣體的質量為0.2g.
(1)反應后溶液中溶質MgCl2的質量為 g.
(2)向反應后的溶液中逐滴加入NaOH溶液,當加入的NaOH溶液質量為20g時,恰好完全反應,此時,生成沉淀的質量為 g
(3)計算所加NaOH溶液的溶質質量分數是多少?
查看答案和解析>>
科目:初中化學 來源:四川省中考真題 題型:計算題
將一定質量金屬Mg和稀鹽酸恰好完全反應,產生氣體的質量為0.2g
(1)反應后溶液中溶質MgCl2的質量為______g。
(2)向反應后的溶液中逐滴加入NaOH溶液,當加入的NaOH溶液質量為20g時,恰好完全反應,此時,生成沉淀的質量為 ___ g
(3)計算所加NaOH溶液的溶質質量分數是多少?
查看答案和解析>>
科目:初中化學 來源: 題型:
將一定質量金屬Mg和稀鹽酸恰好完全反應,產生氣體的質量為0.2g。
(1)反應后溶液中溶質MgCl2的質量為 g。
(2)向反應后的溶液中逐滴加入NaOH溶液,當加入的NaOH溶液質量為20g時,恰好完全反應,此時,生成沉淀的質量為 g
(3)計算所加NaOH溶液的溶質質量分數是多少?
查看答案和解析>>
科目:初中化學 來源:2012年四川省瀘州市中考化學試卷(解析版) 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com