
我市北部山區盛產石灰石,石灰石的主要成分是碳酸鈣。
(1)實驗室中常用石灰石制取二氧化碳,化學的反應方程式為 ;
其中碳酸鈣中鈣元素的質量分數為 。
(2)某校課外活動小組為了解石灰石資源的品質,對當地石材進行化學分析:取12.5g石灰石顆粒樣品,置于燒杯中并加入足量稀鹽酸,充分反應后稱得混合物的總質量減少4.4g。則該石灰石中含碳酸鈣的質量分數是 。
(1)CaCO3 + 2HCl ="==" CaCl2 + H2O + CO2↑ 40% (2)80%
解析試題分析:(1)實驗室中常用石灰石和稀鹽酸反應制取二氧化碳,同時還生成了氯化鈣和水,故反應的化學方程式為CaCO3 + 2HCl = CaCl2 + H2O + CO2↑;根據化合物中某元素的質量分數= ×100%可知,碳酸鈣中鈣元素的質量分數=
×100%可知,碳酸鈣中鈣元素的質量分數=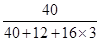 ×100%=40%。
×100%=40%。
(2)根據題意,結合反應的化學方程式可知,充分反應后稱得混合物的總質量減少,是因為反應中有二氧化碳氣體生成并逸出,故減少的4.4g質量即為二氧化碳的質量;再利用化學方程式中碳酸鈣與二氧化碳的質量比,可求出碳酸鈣的質量,進而求出該石灰石中含碳酸鈣的質量分數。
解,設該石灰石中含碳酸鈣的質量為x
CaCO3 + 2HCl = CaCl2 + H2O + CO2↑
100 44
x 4.4g
100:44=x:4.4g
解得,x=10g
所以,該石灰石中含碳酸鈣的質量分數=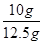 ×100%=80%。
×100%=80%。
答:石灰石中含碳酸鈣的質量分數為80%。
考點:書寫化學方程式,元素的質量分數計算, 根據化學反應方程式的計算
點評:本題為有關化學式的計算,以及根據化學方程式的計算,解題的關鍵是找出相關的化學反應,并根據質量守恒定律判斷出生成二氧化碳的質量,然后依據已知量對未知的應求量進行求解計算即可,注意解題要規范


 天天向上口算本系列答案
天天向上口算本系列答案科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:
我市北部山區盛產石灰石,石灰石的主要成分是碳酸鈣。
(1)實驗室中常用石灰石制取二氧化碳,化學的反應方程式為 ;
其中碳酸鈣中鈣元素的質量分數為 。
(2)某校課外活動小組為了解石灰石資源的品質,對當地石材進行化學分析:取12.5g石灰石顆粒樣品,置于燒杯中并加入足量稀鹽酸,充分反應后稱得混合物的總質量減少了4.4g。則該石灰石中含碳酸鈣的質量分數是 。
查看答案和解析>>
科目:初中化學 來源:2013年廣東省廣州市從化市中考化學一模試卷(解析版) 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com