
【題目】(1)把5.1g鎂鋁合金的粉末放入過量的鹽酸中,得到5.6 LH2(標準狀況下)。
①合金中鎂的物質的量_________。
②寫出該合金溶于足量NaOH溶液的化學方程式_________________。同時產生H2的體積(標準狀況下)為____________ 。
(2)相同條件下,某Cl2與O2混合氣體100 mL恰好與150 mL H2化合生成HCl和H2O,則混合氣體中Cl2與O2的體積比為__________,混合氣體的平均相對分子質量為____________。
(3)兩個相同容積的密閉容器X、Y,在25 ℃下,X中充入a g A氣體,Y中充入a g CH4氣體,X與Y內的壓強之比是4∶11,則A的摩爾質量為____________。
(4)在同溫、同壓下,實驗測得CO、N2和O2三種氣體的混合氣體的密度是H2的14.5倍,其中O2的質量分數為____________ (計算結果保留1位小數) 。若其中CO和N2的物質的量之比為1∶1,則混合氣體中氧元素的質量分數為_______________ (計算結果保留1位小數)。
【答案】0.1 mol 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ 3.36 L 1∶1 27.25 44 g·mol-1 27.6% 48.3%
【解析】
(1)①根據鎂鋁質量和生成氫氣的體積列方程組計算;
②只有鋁與氫氧化鈉反應,進行計算;
(2)列方程組計算,混合氣體的平均相對分子質量等于混合氣體的總質量除以混合氣體的總物質的量所得數值;
(3)根據PV=nRT進行計算;
(4)在同溫、同壓下,密度比等于相對分子質量之比進行計算;混合氣體中氧元素的質量分數為氧元素的質量除以氣體的總質量;
①設鎂、鋁的物質的量分別為 x mol、 y mol,列方程組:
①24x +27y =5.1 ②x + 1.5y =5.6/22.4=0.25,①②聯立得x=0.1mol、y=0.1mol
答案:0.1mol
②寫出該合金溶于足量NaOH溶液的化學方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑。
因為2Al~3H2,前面已經算出Al的物質的量為0.1mol,則V(H2)=0.1mol×3/2×22.4L/mol=3.36L;
答案:2Al+2NaOH+2H2O=2NaAlO2+3H2↑ 3.36L。
(2)設氯氣為xml,氧氣為yml
Cl2 + H2![]() 2HCl,2H2 + O2
2HCl,2H2 + O2![]() 2H2O
2H2O
xml xml 2yml yml
①x+y=100 ② x+2y=150,①②兩個方程聯立可得x=y=50ml,
假設氯氣和氧氣各1摩爾,則混合氣體的平均摩爾質量為:![]() =51.5g/mol,則混合氣體的平均相對分子質量為51.5;
=51.5g/mol,則混合氣體的平均相對分子質量為51.5;
答案:1:1;51.5
(3)(1)根據PV=nRT,在T、V相同時,壓強之比等于物質的量之比,即4:11=![]() :
:![]() ,解得:M=44g/mol;
,解得:M=44g/mol;
答案:44g/mol。
(4)混合氣體的密度是H2的14.5倍,平均相對分子質量=14.5×2=29,由于CO,N2相對分子質量都是28,所以可以設CO,N2總物質的量為x,O2物質的量為y,則28x+32y=29×(x+y),解得x:y=3:1,所以O2的質量分數=32/(29×4)=27.6%
若其中CO和N2的物質的量之比為1:1,假設CO為1mol,氮氣為1mol,氧氣為(1+1)×1/3=2/3mol,則混合氣體中氧元素的質量分數= ×100%=48.3%;
×100%=48.3%;
答案:27.6% 48.3%


科目:高中化學 來源: 題型:
【題目】2 L密閉容器中進行反應:pZ(g)+qQ(g) ![]() mX(g)+nY(g),式中m、n、p、q為化學計量數。在0~3 min內,各物質的物質的量的變化如下表所示:
mX(g)+nY(g),式中m、n、p、q為化學計量數。在0~3 min內,各物質的物質的量的變化如下表所示:
物質 | X | Y | Z | Q |
起始/mol | 0.7 | 1 | ||
2 min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
3 min末/mol | 0.8 |
已知:2 min內v(Q)=0.075 mol·L-1·min-1,v(Z)∶v(Y)=1∶2。
請回答下列問題:
(1)2 min內X的反應速率v(X)=__________。
(2)起始時n(Y)=__________。
(3) 3 min末是否達到平衡_______(填是或否)。
(4)對于該反應,能增大正反應速率的措施是________(填序號,下同)。
A.縮小容器體積 B.移走部分Q
C.通入大量He氣 D.升高溫度
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求填寫下列空白
如下圖所示,a、b均為活塞,可控制氣體的通過和液體的加入,實驗前活塞均已關閉(儀器的固定裝置已省略)。請選擇最適宜的試劑,利用下圖,把一定量的CO2和CO混合氣體中的CO2和CO分離。可供選擇的試劑有:濃硫酸、稀硫酸、濃鹽酸、稀鹽酸、氫氧化鈉溶液、紫色石蕊試液。

(1)甲裝置的燒瓶中盛放的試劑是_____________,分液漏斗中盛放的試劑是__________;
(2)乙裝置的瓶中盛放的試劑是_______________。
(3)打開活塞a時,分離出來的氣體是________;要得到另一種氣體時,正確的操作是_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知Fe3O4可表示成FeO·Fe2O3,水熱法制備Fe3O4納米顆粒的總反應為:3Fe2++2S2O32-![]() +O2+4OH-
+O2+4OH-![]() Fe3O4+S4O62-
Fe3O4+S4O62-![]() +2H2O。下列說法正確的是( )
+2H2O。下列說法正確的是( )
A. O2和S2O32-是氧化劑,Fe2+是還原劑
B. 若有2 mol Fe2+被氧化,則被Fe2+還原的O2為0.5 mol
C. 每生成1 mol Fe3O4 ,轉移電子的物質的量為2 mol
D. 參加反應的氧化劑與還原劑的物質的量之比為1∶1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】把一塊鎂鋁合金投入到1 mol/L酸中,待合金完全溶解后,再往溶液里加入1 mol/L NaOH溶液,生成沉淀的物質的量隨加入NaOH溶液的體積變化的關系如下圖所示,下列說法中錯誤的是( )

A. 鹽酸的體積為80mlB. a的取值范圍為0≤ a <50
C. n(Mg2+)<0.025molD. 當a值為30時,b值為0.01
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A. 乙烯使溴水或酸性高錳酸鉀褪色均屬于加成反應
B. 利用溴水能鑒別苯、乙醇和乙酸三種溶液
C. 用重鉻酸鉀溶液檢驗司機是否酒駕所發生的反應屬于乙醇的氧化反應
D. 石油的分餾、煤的干餾都是物理變化,而裂化、裂解是化學變化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】制得的碳酸鈉樣品中往往含有少量NaCl,現欲測定樣品中Na2CO3的質量分數,某探究性學習小組分別設計了如下實驗方案。請回答下列有關問題:
方案一:把一定質量的樣品溶解后加入過量的CaCl2溶液,將所得沉淀____________(填操作名稱)、洗滌、烘干、稱量、計算。洗滌沉淀的具體操作是_____________________________。
方案二:把一定量的樣品與足量硫酸反應后,用下圖所示裝置測定產生CO2的體積,為了確保測定結果的準確性,B中的溶液最好采用_________________。下圖裝置中實驗儀器a的名是_________________。

方案三:利用如圖所示裝置來測定純堿樣品中碳酸鈉的質量分數(鐵架臺、鐵夾等在圖中均已略去)。實驗步驟如下:
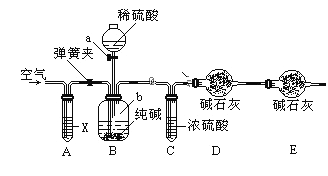
①按圖連接裝置,并檢查氣密性;
②準確稱得盛有堿石灰的干燥管D的質量為33.4g;
③準確稱得6g純堿樣品放入容器b中;
④打開分液漏斗a的旋塞,緩緩滴入稀硫酸,至不再產生氣泡為止;
⑤打開彈簧夾,往試管A中緩緩鼓入空氣數分鐘,然后稱得干燥管D的總質量為35.6g。
(1)若④⑤兩步的實驗操作太快,則會導致測定結果__________(填“偏大”或“偏小”)。
(2)裝置A中試劑X應選用________________________。
(3)E裝置的作用是_______________________________。
(4)根據實驗中測得的有關數據,計算純堿樣品Na2CO3的質量分數為___________(結果保留小數點后一位)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據下圖兩套基礎實驗裝置回答問題。
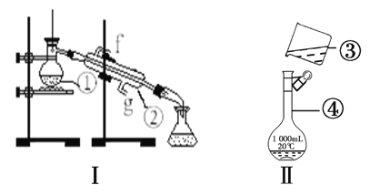
(1)寫出下列儀器的名稱:______________、___________________。
(2)儀器①~④中,使用時必須檢查是否漏水的有____________________。(填序號)
(3)用裝置I制蒸餾水,還缺少的儀器有_________,冷卻水從_______口進。
(4)a.現需配制250mL0.2molL-1NaCl溶液,其中裝置II是某同學配制此溶液時轉移操作的示意圖,圖中有兩處錯誤分別是_______________,_______________。
b.配制過程中,下列情況會使配制結果偏高的是________________(填序號)。
①定容時俯視刻度線觀察液面;②容量瓶使用時未干燥;③定容后經振蕩、搖勻、靜置,發現液面低于刻度線,再加蒸餾水補至刻度線;④移液時未洗滌燒杯和玻璃棒
c.若實驗中加蒸餾水時不慎超過了刻度,應如何處理?______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列裝置可以用于NH3、SO2等氣體的制備。

請回答下列問題:
(1)若用Ca(OH)2固體和NH4Cl固體制取少量NH3,則選用的裝置是_____(填序號)產生NH3的化學方程式為__________________________________,干燥NH3可以用____________(試劑名稱),檢驗集氣瓶中是否收集滿氨氣的方法是____________________________________。
(2)若用銅與濃硫酸反應制取SO2,應選用裝置________(填序號),產生SO2的化學方程式為_____________________________________________________。(填序號)
下列溶液能直接用于檢驗SO2氣體存在的是__________。
A.酸性KMnO4溶液 B.NaOH溶液 C.Na2CO3溶液 D.品紅溶液
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com