
題目列表(包括答案和解析)
| 溫度 | NH4Cl | NH4HCO3 | NaHCO3 | NaCl |
| 30℃ | 41.1g | 27.0g | 11.1g | 36.3g |
| ||

| 物質 | NaCl | NH4CO3 | NH4Cl | NaHCO3 |
| 溶解度 | 36.0 | 21.6 | 37.2 | 9.6 |

海洋是個巨大的寶庫,為人類提供了寶貴的自然資源。
(1)食用海魚攝取的主要營養素是 。
(2)右圖為海水淡化裝置,利用的能源是 ,獲得的蒸餾水屬于 (填字母序號)。

A.單質 B.化合物 C.混合物
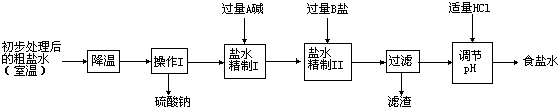
(3)利用海水可制取許多化工產品。用海水制食鹽,常通過海水曬鹽得到粗鹽,粗鹽中含有少量的CaCl2、Na2SO4等雜質。 除去上述雜質,先加過量BaCl2溶液除去 ,再加過量 溶液除去CaCl2和過量的BaCl2,生成的沉淀經 除去,最后加入 調節pH,蒸發,結晶,制得精鹽。
(4)用氯化鈉和碳酸氫銨NH4HCO3可制備碳酸氫鈉和氯化銨NH4Cl,該反應化學方程式可表示為:NaCl+ NH4HCO3=NaHCO3+NH4Cl。
20℃時,按上述化學方程式中反應物的質量比,向100 g水中加入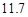 g
NaCl和
g
NaCl和 g NH4HCO3,理論上從溶液中析出晶體的質量為 g。
g NH4HCO3,理論上從溶液中析出晶體的質量為 g。
資料:20℃時四種物質的溶解度如下,假設它們同時溶解在水中各自的溶解度不變。
|
物質 |
NaCl |
NH4HCO3 |
NH4Cl |
NaHCO3 |
|
溶解度/g |
|
|
|
|
(5)從海水中提取溴常用吹出法,即用氯氣(C12)將海水里溴化鈉(NaBr)中的溴置換出來,再用空氣或水蒸氣吹出溴(Br2)。流程示意圖如下:
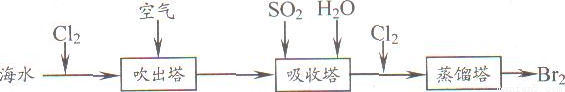
①寫出氯氣置換出溴單質的化學方程式: ;該反應在pH=3的酸性條件下進行,可用 測定反應液的酸堿度。
②吹出的溴和大量空氣混合在一起進入吸收塔(吸收塔中發生的反應:Br2+SO2+2H2O==H2SO4+2HBr)。根據流程圖分析,通入SO2的目的是 。
(8分)(2012?南通)海洋是個巨大的資源寶庫,利用海水可制取許多化工產品.
(1)用海水制食鹽,常通過 _________ 得到粗鹽,粗鹽中含有少量的CaCl2、Na2S04等雜質.除去上述雜質,先加過量BaCl2溶液除去 _________ ,再加 _________ 溶液除去CaCl2和過量的BaCl2,生成的沉淀經 _________ 除去.
(2)從海水中提取溴常用吹出法,即用氯氣(C12)將海水里溴化鈉(NaBr)中的溴置換出來,再用空氣或水蒸氣吹出溴(Br2).流程示意圖如下:
①寫出氯氣置換出溴單質的化學方程式: _________ ;該反應在pH=3的酸性條件下進行,可用 _________ 測定反應液的酸堿度.
②吹出的溴和大量空氣混合在一起進入吸收塔(吸收塔中發生的反應:Br2+S02+2H20═H2S04+2HBr).根據流程圖分析,通入S02的目的是 _________ .
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com