三(11)班學生將采集到的樣品用水沖洗后晾干,獲得了25.0g塊狀石灰石樣品.班級甲、乙兩組同學共利用這25.0g石灰石樣品分別進行了如下實驗.(假設樣品中其他雜質不參加反應,不考慮水、氯化氫逸出)
[實驗過程]
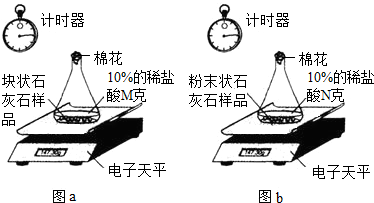
甲組:取一定質量的塊狀石灰石樣品于錐形瓶內,并加入10%的稀鹽酸Mg,恰好完全反應.(如圖a)
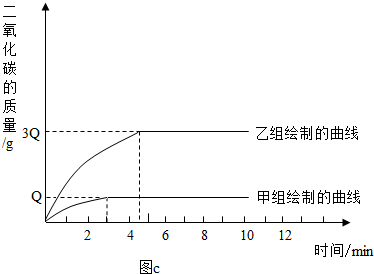
乙組:先把剩余的塊狀石灰石樣品研碎成粉末狀,然后全部置于錐形瓶內,并加入10%的稀鹽酸Ng,也恰好完全反應.(如圖b)
[數據處理]
(1)甲、乙兩組同學所用稀鹽酸的總質量:M+N=146g.
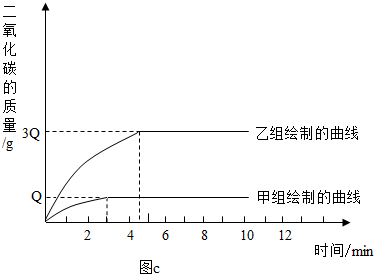
(2)兩組同學經數據處理得到釋放出二氧化碳的質量與反應時間的關系如下圖c
[問題討論]
(1)甲、乙兩組同學的實驗中,______組實驗消耗的時間更短.
(2)圖c中的數據Q等于______g,甲、乙兩組實驗中共產生二氧化碳氣體______g,兩次實驗中消耗的稀鹽酸質量比M:N=______.
(3)求石灰石樣品中碳酸鈣的質量分數.