
題目列表(包括答案和解析)
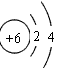 是碳原子結構示意圖,碳原子的最外層電子數是 ,碳元素在元素周期表中位于第 周期。
是碳原子結構示意圖,碳原子的最外層電子數是 ,碳元素在元素周期表中位于第 周期。 
碳與碳的化合物在工農業生產及日常生活中有廣泛的用途。
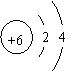 (1)右圖是碳原子結構示意圖,碳原子的最外層電子數是 ,碳元素在元素周期表中位于第 周期。
(1)右圖是碳原子結構示意圖,碳原子的最外層電子數是 ,碳元素在元素周期表中位于第 周期。
(2) 古代用墨書寫或繪制的字畫雖年久仍不變色,原因是墨中主要成分碳在常溫下具有 性。右圖是木炭還原氧化銅的實驗,大試管中的反應體現了碳的還原性,單質碳的還原性可以用于冶金工業。①酒精燈加燈罩的目的 ;②剛開始預熱,試管②中立即產生氣泡,但石灰水不變渾濁,原因是 ;
③繼續加熱,觀察到石灰水逐漸變渾濁,黑色粉末中出現 紅色物質。請你寫出帶點部分的化學方程式:
。
④停止加熱時,應先將導管從試管②中撤出,待試管①冷卻后再把試管里的粉末倒出。這樣操作的原因是 A ;
B 。
(3) 二氧化碳能參與光合作用完成大氣中的“碳循環”,但是大氣中二氧化碳的含量不斷上升,會使全球變暖,從而導致 。蔬菜大棚用作氣肥的二氧化碳,可用多種方法制得,例如可以用稀硫酸與碳酸氫銨(NH4HCO3)反應制得,反應后生成硫酸銨、水和二氧化碳,這一反應的化學方程式是 。
(4) 研究發現:物質的結構決定性質,物質的性質決定用途。如:一氧化碳也能還原氧化銅,也有還原性。從化學反應前后碳元素化合價的變化特點分析,一氧化碳和碳都具有還原性的原因是 。

做完“鐵在氧氣里燃燒”實驗后,小冬同學有兩個疑惑不解的問題,于是她進行了以下探究活動,請你一同參與。
[問題1]鐵燃燒時濺落下來的黑色物質中還有沒有鐵呢?
[查閱資料1]
(1) 自然界中鐵的氧化物主要是Fe3O4和Fe2O3兩種(FeO極易被氧化為Fe2O3);
(2) 鐵的氧化物均能溶于酸的溶液。
[實驗探究]
將冷卻后的黑色物質碾碎,裝入試管,加入_____溶液,觀察到的現象是_____,說明鐵燃燒時濺落下來的黑色物質中還含有鐵。
[問題2]鐵燃燒的產物為什么不是Fe2O3呢?
[查閱資料2]
(1) Fe3O4和Fe2O3的分解溫度、鐵的熔點見表:
(2) Fe2O3高溫時分解成Fe3O4。
[理論探討]
根據實驗現象,并結合表中數據,可推知鐵在氧氣里燃燒時產生的高溫應在_____之間,在此溫度范圍內Fe2O3已分解,所以鐵在氧氣里燃燒的產生是Fe3O4。
[拓展延伸]
(1) 實驗中為了防止集氣瓶炸裂,必須_____;
(2) Fe2O3高溫時會分解成Fe3O4和一種氣體,請寫出此反應的化學方程式__________;
(3) 有些超市的食品密封包裝盒的透明蓋內放有黑色的FeO粉末,若粉末的顏色_____,就說明包裝盒破損進氣,這樣售貨員就能及時發現并處理。
| Fe3O4 | Fe2O3 | 鐵 | |
| 分解溫度/℃ | 1538 | 1400 | — |
| 熔點/℃ | — | — | 1535 |
做完“鐵在氧氣里燃燒”實驗后,小冬同學有兩個疑惑不解的問題,于是她進行了以下探究活動,請你一同參與。
[問題1]鐵燃燒時濺落下來的黑色物質中還有沒有鐵呢?
[查閱資料1]
(1) 自然界中鐵的氧化物主要是Fe3O4和Fe2O3兩種(FeO極易被氧化為Fe2O3);
(2) 鐵的氧化物均能溶于酸的溶液。
[實驗探究]
將冷卻后的黑色物質碾碎,裝入試管,加入_____溶液,觀察到的現象是_____,說明鐵燃燒時濺落下來的黑色物質中還含有鐵。
[問題2]鐵燃燒的產物為什么不是Fe2O3呢?
[查閱資料2]
(1) Fe3O4和Fe2O3的分解溫度、鐵的熔點見表:
(2) Fe2O3高溫時分解成Fe3O4。
[理論探討]
根據實驗現象,并結合表中數據,可推知鐵在氧氣里燃燒時產生的高溫應在_____之間,在此溫度范圍內Fe2O3已分解,所以鐵在氧氣里燃燒的產生是Fe3O4。
[拓展延伸]
(1) 實驗中為了防止集氣瓶炸裂,必須_____;
(2) Fe2O3高溫時會分解成Fe3O4和一種氣體,請寫出此反應的化學方程式__________;
(3) 有些超市的食品密封包裝盒的透明蓋內放有黑色的FeO粉末,若粉末的顏色_____,就說明包裝盒破損進氣,這樣售貨員就能及時發現并處理。
| Fe3O4 | Fe2O3 | 鐵 | |
| 分解溫度/℃ | 1538 | 1400 | — |
| 熔點/℃ | — | — | 1535 |
做完“鐵在氧氣里燃燒”實驗后,某興趣小組有一些疑惑不解的問題,于是他們進行了以下探究活動,請你一同參與。
[問題1] 細鐵絲在氧氣中燃燒為什么會“火星四射”?
[查閱資料1]①日常生活中的鋼鐵制品都含有少量碳雜質。 ②含碳細鐵絲燃燒時,其中的炭粒生成的CO2氣體在熔融液態物質中形成氣泡,熔融液態物質因氣泡炸裂引起“火星四射”的現象。
[設計實驗]為了探究細鐵絲在純氧中燃燒產生“火星四射”現象的原因,該小組同學設計的實驗方案是:取長短粗細相同的含碳細鐵絲和不含碳的細鐵絲,分別在足量的氧氣中燃燒,觀察現象。你認為他們的方案 (填“合理”或“不合理”)。
 [實驗探究1]小明做細鐵絲在氧氣中的燃燒實驗時,他把細鐵絲繞成螺旋狀,一端系在一根鐵絲上,另一端系上一根火柴。點燃火柴后迅速把鐵絲連同火柴一起插入集氣瓶下部(沒有接觸到細沙,如圖所示),但不見鐵絲燃燒,反復實驗均未成功。
[實驗探究1]小明做細鐵絲在氧氣中的燃燒實驗時,他把細鐵絲繞成螺旋狀,一端系在一根鐵絲上,另一端系上一根火柴。點燃火柴后迅速把鐵絲連同火柴一起插入集氣瓶下部(沒有接觸到細沙,如圖所示),但不見鐵絲燃燒,反復實驗均未成功。
該同學認為可能導致失敗的原因主要有三種:
A.鐵絲表面有銹跡,影響了反應的進行;
B.點燃火柴后立即將它伸入瓶內,火柴燃燒消耗了氧氣,不利于鐵絲 的燃燒;
C.火柴燃燒時有大量的熱量放出,將鐵絲和火柴迅速伸至集氣瓶下部,因熱脹冷縮之故。瓶內氧氣會膨脹逸出,使鐵絲無法燃燒。
實驗:根據以上假設,他對實驗應作的相應改進為:
(1) ;(2) ;(3) 。
[問題2]鐵燃燒時濺落下來的黑色物質中還有沒有鐵呢?
[查閱資料2] ①自然界中鐵的氧化物主要是Fe3O4和Fe2O3兩種(FeO極易被氧化為Fe2O3);②鐵的氧化物均能溶于酸的溶液。
[實驗探究2]將冷卻后的黑色物質碾碎,裝入試管,加入_____溶液,觀察到的現象是_____,說明鐵燃燒時濺落下來的黑色物質中還含有鐵。
[問題3]鐵燃燒的產物為什么不是Fe2O3呢?
[查閱資料3]①Fe3O4和Fe2O3的分解溫度、鐵的熔點見表:②Fe2O3高溫時分解成Fe3O4。
[理論探討]
根據實驗現象,并結合表中數據,可推知鐵在氧氣里燃燒時產生的高溫應在_____之間,在此溫度范圍內Fe2O3已分解,所以鐵在氧氣里燃燒的產生是Fe3O4。
[拓展延伸]
(1)小林同學發現“鐵絲”在純凈氧氣中燃燒起來,觀察到火星四射,并有黑色固體生成,請寫出該反應的化學方程式 ;
(2)Fe2O3高溫時會分解成Fe3O4和一種氣體,請寫出此反應的化學方程式__________;
(3)有些超市的食品密封包裝盒的透明蓋內放有黑色的FeO粉末,若粉末的顏色_____,就說明包裝盒破損進氣,這樣售貨員就能及時發現并處理。
| Fe3O4 | Fe2O3 | 鐵 | |
| 分解溫度/℃ | 1538 | 1400 | — |
| 熔點/℃ | — | — | 1535 |
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com