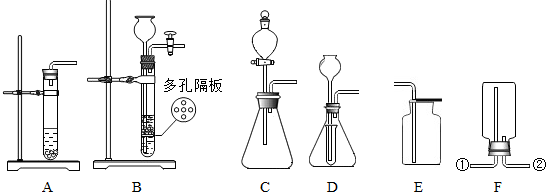
實驗室用鹽酸和碳酸鈣固體反應,將得到的氣體X通入澄清石灰水中,始終沒有發現石灰水變渾濁.為此,同學們進行了探究.
[提出猜想]甲同學認為:澄清石灰水已變質; 乙同學認為:氣體X中不只含有CO
2;
[實驗方案]
(1)甲的探究:①取稀硫酸與碳酸鈉反應制取CO
2;反應的方程式為
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
,將生成的氣體通入澄清石灰水.
現象為
澄清的石灰水變渾濁
澄清的石灰水變渾濁
.
實驗結論:澄清石灰水沒有變質.
(2)乙的探究:用鹽酸和碳酸鈣固體反應,將得到的氣體X通入硝酸銀溶液.
實驗現象
有白色沉淀生成
有白色沉淀生成
;
實驗結論:氣體X中還有
HCl
HCl
氣體.根據實驗結論,用化學方程式表示石灰水未變渾濁的原因
CaCO3+2HCl=CaCl2+CO2↑+H2O;Ca(OH)2+2HCl=CaCl2+2H2O
CaCO3+2HCl=CaCl2+CO2↑+H2O;Ca(OH)2+2HCl=CaCl2+2H2O
.
[分析與討論]
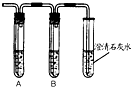
(3)在討論中,丙同學提出:只用圖25實驗裝置就可以同時完成上述兩個假設的探究.則A、B試管中的試劑依次是下列選項中的
②
②
.
①濃硫酸、硝酸銀溶液
②飽和碳酸氫鈉溶液、硝酸銀溶液
③硝酸銀溶液、石蕊溶液
④氫氧化鈉溶液、硝酸銀溶液
(4)B試管中試劑的作用是
檢驗HCl是否除盡
檢驗HCl是否除盡
.

 實驗室用鹽酸和碳酸鈣固體反應,將得到的氣體X通入澄清石灰水中,始終沒有發現石灰水變渾濁.為此,同學們進行了探究.
實驗室用鹽酸和碳酸鈣固體反應,將得到的氣體X通入澄清石灰水中,始終沒有發現石灰水變渾濁.為此,同學們進行了探究.