
題目列表(包括答案和解析)
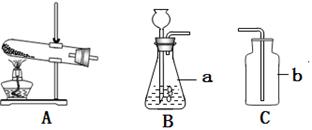
圖所示為實驗室常用的實驗裝置,據此回答下列問題:
(1)寫出標號所示儀器的名稱
b 。
 |
(2)實驗室用高錳酸鉀制取氧氣的反應表達式為 。
小明同學打算從制取O2后的固體殘渣中回收二氧化錳(固體殘渣中只有MnO2不溶于水)的方法是溶解、 、洗滌并干燥。
(3)收集二氧化碳只能用C裝置的原因是 。
(4)小雯發現在加熱硬水的過程中,產生了一種難溶性的固體。
提出猜想: 難溶性的固體可能是碳酸鈣。向這種難溶性的固體中滴入稀鹽酸稀鹽酸
,觀察到有大量的氣泡產生,則這種固體可 能是碳酸鈣;若這種固體是碳酸鈣,寫出該反應的表達式 CaCO3+2HCl═CaCl2+H2O+CO2↑。
能是碳酸鈣;若這種固體是碳酸鈣,寫出該反應的表達式 CaCO3+2HCl═CaCl2+H2O+CO2↑。
 (5)下圖是小雯用這種固體制取CO2,并驗證CO2性質的實驗組合裝置,根據裝置解答下列問題:
(5)下圖是小雯用這種固體制取CO2,并驗證CO2性質的實驗組合裝置,根據裝置解答下列問題:
①方框中的發生裝置應選擇本題上右圖中 (選填:A、B)裝置;
②在裝置D中可觀察到的實驗現象是:___ __,其相關的反應表達式為: ;
③裝置E通常用于實驗室檢驗CO2氣體,現象是:________ _____________;
④裝置F中可觀察到奇妙的現象,從而說明CO2可用于:________  _____________;
_____________;
⑤實驗室要制取NO2氣體做微粒運動的演示實驗。NO2是一種紅棕色的氣體,密度比空氣大,易被氫氧化鈉溶液吸收,能與水反應生成硝酸和NO;NO2和NO都有毒,易污染環境。
Ⅰ.收集NO2可用如圖1所示的裝置,NO2應從端__ __(填“a”或“b”)通入。
Ⅱ.實驗室通常在收集裝置后還連接一套圖2所示的裝置,你認為這套裝置的主要作用是:
Ⅲ.如圖3,做微粒運動演示實驗時,為縮短演示時間,NO2最好盛放在 (填“上”或“下”)面的集氣瓶中,另一瓶放空氣。抽去玻璃片可看到: 。
 |
(14分)如圖所示為實驗室常用的實驗裝置,據此回答下列問題:
(1)寫出標號所示儀器的名稱b 。
(2)實驗室用高錳酸鉀制取氧氣的反應表達式為 。
小明同學打算從制取O2后的固體殘渣中回收二氧化錳(固體殘渣中只有MnO2不溶于水)的方法是溶解、 、洗滌并干燥。
(3)收集二氧化碳只能用C裝置的原因是 。
(4)小雯發現在加熱硬水的過程中,產生了一種難溶性的固體。提出猜想: 難溶性的固體可能是碳酸鈣。向這種難溶性的固體中滴入稀鹽酸稀鹽酸,觀察到有大量的氣泡產生,則這種固體可能是碳酸鈣;若這種固體是碳酸鈣,寫出該反應的表達式 。
(5)如圖是小雯用這種固體制取CO2,并驗證CO2性質的實驗組合裝置,根據裝置解答下列問題:
①方框中的發生裝置應選擇本題上右圖中 (選填:A、B)裝置;
②在裝置D中可觀察到的實驗現象是:___ __,其相關的反應表達式為: ;
③裝置E通常用于實驗室檢驗CO2氣體,現象是:________ _____________;
④裝置F中可觀察到奇妙的現象,從而說明CO2可用于:________ _____________;
⑤實驗室要制取NO2氣體做微粒運動的演示實驗。NO2是一種紅棕色的氣體,密度比空氣大,易被氫氧化鈉溶液吸收,能與水反應生成硝酸和NO;NO2和NO都有毒,易污染環境。
Ⅰ.收集NO2可用如圖1所示的裝置, NO2應從端__ __(填“a”或“b”)通入。
Ⅱ.實驗室通常在收集裝置后還連接一套圖2所示的裝置,你認為這套裝置的主要作用是:
Ⅲ.如圖3,做微粒運動演示實驗時,為縮短演示時間,NO2最好盛放在 (填“上”或“下”)面的集氣瓶中,另一瓶放空氣。抽去玻璃片可看到: 。
(14分)如圖所示為實驗室常用的實驗裝置,據此回答下列問題:

(1)寫出標號所示儀器的名稱b 。
(2)實驗室用高錳酸鉀制取氧氣的反應表達式為 。
小明同學打算從制取O2后的固體殘渣中回收二氧化錳(固體殘渣中只有MnO2不溶于水)的方法是溶解、 、洗滌并干燥。
(3)收集二氧化碳只能用C裝置的原因是 。
(4)小雯發現在加熱硬水的過程中,產生了一種難溶性的固體。提出猜想: 難溶性的固體可能是碳酸鈣。向這種難溶性的固體中滴入稀鹽酸稀鹽酸,觀察到有大量的氣泡產生,則這種固體可能是碳酸鈣;若這種固體是碳酸鈣,寫出該反應的表達式 。
(5)如圖是小雯用這種固體制取CO2,并驗證CO2性質的實驗組合裝置,根據裝置解答下列問題:

①方框中的發生裝置應選擇本題上右圖中 (選填:A、B)裝置;
②在裝置D中可觀察到的實驗現象是:___ __,其相關的反應表達式為: ;
③裝置E通常用于實驗室檢驗CO2氣體,現象是:________ _____________;
④裝置F中可觀察到奇妙的現象,從而說明CO2可用于:________ _____________;
⑤實驗室要制取NO2氣體做微粒運動的演示實驗。NO2是一種紅棕色的氣體,密度比空氣大,易被氫氧化鈉溶液吸收,能與水反應生成硝酸和NO;NO2和NO都有毒,易污染環境。

Ⅰ.收集NO2可用如圖1所示的裝置, NO2應從端__ __(填“a”或“b”)通入。
Ⅱ.實驗室通常在收集裝置后還連接一套圖2所示的裝置,你認為這套裝置的主要作用是:
Ⅲ.如圖3,做微粒運動演示實驗時,為縮短演示時間,NO2最好盛放在 (填“上”或“下”)面的集氣瓶中,另一瓶放空氣。抽去玻璃片可看到: 。


課外化學興趣小組的同學利用某化工廠的廢堿液(主要成分為Na2CO3、還含有少量NaCl,其它雜質不計)和石灰乳(氫氧化鈣的懸濁液)為原料制備燒堿,并對所得的燒堿粗產品的成分進行分析和測定。
【粗產品制備】
(1)將廢堿液加熱蒸發濃縮,形成較濃的溶液,冷卻后與石灰乳混合,發生反應的化學方程式為 ▲ 。
(2)將反應后的混合物過濾,得到的濾液進行蒸發結晶,制得NaOH粗產品。
【粗產品成分分析】
(1)取適量粗產品溶于水,加入Ba(NO3)2溶液出現白色渾濁,發生反應的化學方程式為 ▲ ,該粗產品中一定不含有 ▲ ,理由是 ▲ 。
(2)該小組同學通過對粗產品成分的實驗分析,確定該粗產品中含有三種物質。
【粗產品含量測定】
Na2CO3含量的測定:
(1)該興趣小組的同學設計了下圖所示的實驗裝置。取20.0g粗產品,進行實驗。

【說明】①堿石灰是CaO與NaOH的固體混合物。
②E裝置中的飽和NaHCO3溶液是為了除去二氧化碳氣體中的氯化氫,發生
的反應為:NaHCO3+ HCl = NaCl + CO2 ↑ + H2O。
(2)操作步驟
①連接好裝置,檢查氣密性;
②打開彈簧夾C,在A處緩緩通入一段時間空氣;
③稱量G的質量;
④關閉彈簧夾C,慢慢滴加濃鹽酸至過量,直至D中無氣泡冒出;
⑤打開彈簧夾C,再次緩緩通入一段時間空氣;
⑥再次稱量G的質量,得前后兩次質量差為4.8g。
(3)問題探究
①F中的試劑應為 ▲ 。
②B裝置的作用是 ▲ ,H裝置的作用是 ▲ 。
③若沒有H裝置,則測定的Na2CO3的質量分數會 ▲ (填“偏大”、“偏小”、“不變”)。
事實上20.0 g粗產品只能產生4.4 g CO2 。請你仔細分析上述實驗,解釋實驗值4.8g比正確值4.4 g偏大的原因(假設操作均正確) ▲ 。
(4)數據計算
根據正確值4.4 g可求得粗產品中Na2CO3的質量分數為 ▲ %。
NaOH含量的測定:
該小組同學又另取20.0g粗產品,逐滴加入20%的鹽酸至恰好完全反應時,消耗鹽酸的質量為73 g,放出CO2 4.4 g(不考慮二氧化碳氣體的溶解)。求原粗產品中NaOH的質量分數。(寫出計算過程)
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com