
題目列表(包括答案和解析)
 2C2H5OH+2A
2C2H5OH+2A| 實驗方案 | 實驗現象 | |
| 甲 | 取少量黑色物質用磁鐵吸引 | 黑色物質全部被磁鐵吸引 |
| 乙 | 取少量黑色物質加入30%熱的鹽酸中 | 無氣泡、溶液顏色變成黃綠色 |
| 丙 | 取少量黑色物質加入硫酸銅溶液中 | 無任何現象 |
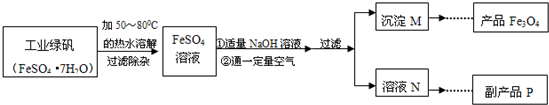
| 溫度/℃ | 0 | 10 | 30 | 50 | 60 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.3 | 33.0 | 30.5 | 27.0 |
| ||
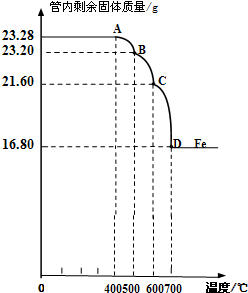 質量差會偏小而影響計算、分析,你認為他們的理由是
質量差會偏小而影響計算、分析,你認為他們的理由是
| ||
| ||
.(10揚州27). (15分)疊氮化鈉(NaN3)被廣泛應用于汽車安全氣囊,某興趣小組對其進行下列研究.
【應用研究】
(1)汽車經撞擊后,30毫秒內引發NaN3,迅速分解為Na、N2,反應方程式為_______。
【制備研究】
(2)將金屬鈉與液態氨反應得NaNH2,再將NaNH2與N2O反應可生成NaN3、NaOH和氣體X,該反應的化學方程式為2NaNH3+N2O = NaN3+NaOH+X,實驗室檢驗X氣體使用的試紙是濕潤________。
【Na2CO3質量分數測定】
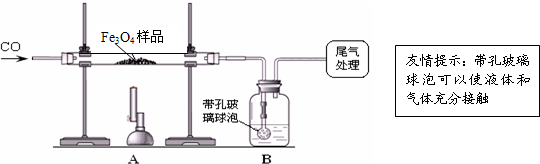
工業級NaN3中常含有少量的Na2CO3,為測定樣品中Na2CO3的質量分數設計如圖
裝置(已知H2SO4溶液與NaN3,反應不生成氣體)。
(3)裝置A的作用是_____。設計的實驗步驟為:①精確稱量樣品,檢查裝置氣密性;②打開彈簧夾,鼓入空氣,稱量裝置C;③關閉彈簧夾,打開分液漏斗活塞;④再打開彈簧夾,_______;⑤再次稱量裝置C。計算碳酸鈉含量至少需要測定______(填數字)個數據。根據制備反應,分析工業級NaN3中含有Na2CO3的可能原因_______。
【NaN3純度測定】精確稱量0.140 g NaN3樣品,設計如圖裝置,測定其純度。已知(NaN3中的N全部轉化為N2,其他產物略),反應中放出大量的熱。
(4)檢查該裝置氣密性的方法是連接好裝置,從水準瓶注水,量氣管中液面與右邊液面形成高度差,做好標記,一段時間后,兩邊高度差_____(填“變大”、“變小”或“不變”),說明氣密性良好。
(5)使小試管中的NaN3樣品與M溶液接觸的操作是______。
(6)使用冷水冷凝的目的是______。反應前應將液面調節到量氣管的“0”刻度,并使兩邊液面相平,反應后讀數時,還需要進行的操作是_______。
(7)常溫下測得量氣管讀數為67.2 mL(N2的密度為1.25 g/L),則實驗中選用的量氣管規格合適的是_____(填字母序號)。
A. 100mL B. 1 L C. 2 L
(8)計算NaN3樣品的純度(寫出計算過程)。

 (NaN3中的N全部轉化為N2,其他產物略),反應中放出大量的熱。
(NaN3中的N全部轉化為N2,其他產物略),反應中放出大量的熱。
.(10揚州27). (15分)疊氮化鈉(NaN3)被廣泛應用于汽車安全氣囊,某興趣小組對其進行下列研究.
【應用研究】
(1)汽車經撞擊后,30毫秒內引發NaN3,迅速分解為Na、N2,反應方程式為_______。
【制備研究】
(2)將金屬鈉與液態氨反應得NaNH2,再將NaNH2與N2O反應可生成NaN3、NaOH和氣體X,該反應的化學方程式為2NaNH3+N2O = NaN3+NaOH+X,實驗室檢驗X氣體使用的試紙是濕潤________。
【Na2CO3質量分數測定】
工業級NaN3中常含有少量的Na2CO3,為測定樣品中Na2CO3的質量分數設計如圖
裝置(已知H2SO4溶液與NaN3,反應不生成氣體)。
(3)裝置A的作用是_____。設計的實驗步驟為:①精確稱量樣品,檢查裝置氣密性;②打開彈簧夾,鼓入空氣,稱量裝置C;③關閉彈簧夾,打開分液漏斗活塞;④再打開彈簧夾,_______;⑤再次稱量裝置C。計算碳酸鈉含量至少需要測定______(填數字)個數據。根據制備反應,分析工業級NaN3中含有Na2CO3的可能原因_______。
【NaN3純度測定】精確稱量0.140 g NaN3樣品,設計如圖裝置,測定其純度。已知 (NaN3中的N全部轉化為N2,其他產物略),反應中放出大量的熱。
(NaN3中的N全部轉化為N2,其他產物略),反應中放出大量的熱。
(4)檢查該裝置氣密性的方法是連接好裝置,從水準瓶注水,量氣管中液面與右邊液面形成高度差,做好標記,一段時間后,兩邊高度差_____(填“變大”、“變小”或“不變”),說明氣密性良好。
(5)使小試管中的NaN3樣品與M溶液接觸的操作是______。
(6)使用冷水冷凝的目的是______。反應前應將液面調節到量氣管的“0”刻度,并使兩邊液面相平,反應后讀數時,還需要進行的操作是_______。
(7)常溫下測得量氣管讀數為67.2 mL(N2的密度為1.25 g/L),則實驗中選用的量氣管規格合適的是_____(填字母序號)。
A. 100 mL B. 1 L C. 2 L
(8)計算NaN3樣品的純度(寫出計算過程)。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com