
題目列表(包括答案和解析)
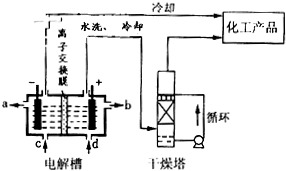
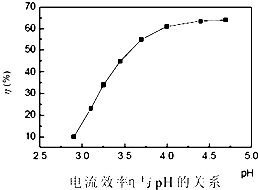 人造金剛石酸洗廢液中含有大量的Ni2+、Mn2+、Co2+等離子.某廠技術人員設計了如下方案,使上述離子的濃度降低到排放標準,且得到了純度較高的鎳粉.
人造金剛石酸洗廢液中含有大量的Ni2+、Mn2+、Co2+等離子.某廠技術人員設計了如下方案,使上述離子的濃度降低到排放標準,且得到了純度較高的鎳粉.| 金屬元素 | Ni | Mn | Co | Fe | Cu | Zn |
| 濃度(g?L-1) | 45 | 15 | 7.5 | ≤0.1 | ≤0.05 | ≤0.05 |
| ||
| ||
| △ |
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| PH | 3.2 | 5.2 | 12.4 |
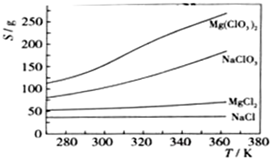
| Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | Mn(OH)2 | |
| 開始沉淀的pH | 7.5 | 2.2 | 5.2 | 6.4 | 8.6 |
| 沉淀完全的pH | 9.0 | 3.2 | 6.7 | 8.0 | 10.1 |
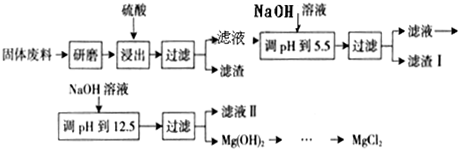
利用含錳廢水(主要含Mn2+、SO42-、H+、Fe2+、Al3+、Cu2+)可制備高性能磁性材料碳酸錳(MnCO3)。其中一種工業流程如下:
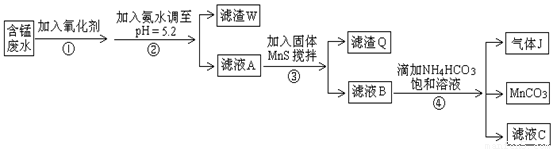
已知某些物質完全沉淀的pH值如下表:
|
沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Cu(OH)2 |
Mn(OH)2 |
CuS |
MnS |
MnCO3 |
|
沉淀完全時的PH |
3.7 |
5.2 |
6.4 |
9.8 |
≥0 |
≥7 |
≥7 |
回答下列問題:
(1)若下列物質均能把Fe2+氧化為Fe3+,則過程①中可選擇加入的氧化劑是 。
a.Cl2 b.MnO2 c.濃HNO3 d.H2O2
(2)過程②中,所得濾渣的成分是 。
(3)過程③中,攪拌的目的是 ,發生反應的離子方程式是 。
(4)過程④中,若生成的氣體J可使澄清石灰水變渾濁,則生成MnCO3反應的離子方程式是___________。
(5)由MnCO3可制得重要的催化劑MnO2,MnCO3 + O2
→ MnO2 + CO2。
O2
→ MnO2 + CO2。
現在空氣中加熱 460.0 g的MnCO3,得到332.0 g產品,若產品中雜質只有MnO,則該產品中MnO2的質量分數是 。(摩爾質量/g·:MnCO3 115 MnO2 87 MnO 71)
(10分)下表為部分短周期元素化合價及相應氫化物沸點的數據:
|
元素性質 |
元素編號 |
|||||||
|
A |
B |
C |
D |
E |
F |
G |
H |
|
|
氫化物的沸點(℃) |
-60.7 |
-33.4 |
-111.5 |
100 |
-87.7 |
19.54 |
-84.9 |
-161.5 |
|
最高化合價 |
+6 |
+5 |
+4 |
|
+5 |
|
+7 |
+4 |
|
最低化合價 |
-2 |
-3 |
-4 |
-2 |
-3 |
-1 |
-1 |
-4 |
已知:①A與D可形成化合物AD2、AD3,可用于制備強酸甲;
②B與D可形成化合物BD、BD2,可用于制備強酸乙。
請回答:
(1)表中屬于第三周期元素的是 (用表中元素編號填寫)。
(2)寫出H的最高價氧化物的電子式: ;
比較A、D、G三種簡單陰離子的半徑大小:r( )>r( )>r( ) (均用實際的元素符號表示)。
(3)由表中D元素和氫元素的原子按1:1組成的常見液態化合物的稀溶液易被催化分解,可使用的催化劑為(填序號)________________。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(4)分子組成為ADG2的物質在水中會強烈水解,產生使品紅溶液褪色的無色氣體和一種強酸。該反應的化學方程式是: 。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com