
題目列表(包括答案和解析)
硅是信息產業、太陽能電池光電轉化的基礎材料。鋅還原四氯化硅是一種有著良好應用前景的制備硅的方法,該制備過程示意如下:

(1)焦炭在過程Ⅰ中作______劑。
(2)過程Ⅱ中的Cl2用電解飽和食鹽水制備,制備Cl2的化學方程式是 。
(3)整個制備過程必須嚴格控制無水。
①SiCl4遇水劇烈水解生成SiO2和一種酸,反應的化學方程式是 。
②干燥Cl2時,從有利于充分干燥和操作安全的角度考慮,需將約90℃的潮濕氯氣先冷卻至12℃,然后再通入到濃H2SO4中。冷卻的作用是 。
(4)Zn還原SiCl4的反應如下:
反應1: 400℃~756℃ ,SiCl4(g) +
2Zn(l)  Si(s)
+ 2ZnCl2(l) ΔH1 <0
Si(s)
+ 2ZnCl2(l) ΔH1 <0
反應2: 756℃~907℃ ,SiCl4(g) +
2Zn(l)  Si(s)
+ 2ZnCl2(g) ΔH2 <0
Si(s)
+ 2ZnCl2(g) ΔH2 <0
反應3:
907℃~1410℃,SiCl4(g) + 2Zn(g)  Si(s) + 2ZnCl2(g) ΔH3
<0
Si(s) + 2ZnCl2(g) ΔH3
<0
① 對于上述三個反應,下列說法合理的是_____。
a.升高溫度會提高SiCl4的轉化率 b.還原過程需在無氧的氣氛中進行
c.增大壓強能提高反應的速率 d.Na、Mg可以代替Zn還原SiCl4
② 實際制備過程選擇“反應3”,選擇的理由是 。
③ 已知Zn(l)=Zn(g) ΔH = +116 KJ/mol 。若SiCl4的轉化率均為90%,每投入1mol SiCl4,“反應3”比“反應2”多放出_____kJ的熱量。
(5)用硅制作太陽能電池時,為減弱光在硅表面的反射,采用化學腐蝕法在其表面形成粗糙的多孔硅層。腐蝕劑常用稀HNO3和HF的混合液。硅表面首先形成SiO2,最后轉化為H2SiF6。用化學方程式表示SiO2轉化為H2SiF6的過程 。
下列表述錯誤的是
A.太陽能電池可采用硅材料制作,其應用有利于環保、節能
B.提前建成的三峽大壩使用了大量水泥,水泥是新型無機非金屬材料
C.用ClO2取代Cl2對飲用水消毒,效果更好
D.“雨后彩虹”“海市蜃樓”既是一種自然現象又是光學現象,也與膠體的知識有關
硅是信息產業、太陽能電池光電轉化的基礎材料。鋅還原四氯化硅是一種有著良好應用前景的制備硅的方法,該制備過程示意如下: 
(1)焦炭在過程Ⅰ中作______劑。
(2)過程Ⅱ中的Cl2用電解飽和食鹽水制備,制備Cl2的化學方程式是 。
(3)整個制備過程必須嚴格控制無水。
①SiCl4遇水劇烈水解生成SiO2和一種酸,反應的化學方程式是 。
②干燥Cl2時,從有利于充分干燥和操作安全的角度考慮,需將約90℃的潮濕氯氣先冷卻至12℃,然后再通入到濃H2SO4中。冷卻的作用是 。
(4)Zn還原SiCl4的反應如下:
反應1: 400℃~756℃ ,SiCl4(g) + 2Zn(l)  Si(s) + 2ZnCl2(l) ΔH1 <0
Si(s) + 2ZnCl2(l) ΔH1 <0
反應2: 756℃~907℃ ,SiCl4(g) + 2Zn(l)  Si(s) + 2ZnCl2(g) ΔH2 <0
Si(s) + 2ZnCl2(g) ΔH2 <0
反應3: 907℃~1410℃,SiCl4(g) + 2Zn(g)  Si(s) + 2ZnCl2(g) ΔH3 <0
Si(s) + 2ZnCl2(g) ΔH3 <0
① 對于上述三個反應,下列說法合理的是_____。
a.升高溫度會提高SiCl4的轉化率 b.還原過程需在無氧的氣氛中進行
c.增大壓強能提高反應的速率 d.Na、Mg可以代替Zn還原SiCl4
② 實際制備過程選擇“反應3”,選擇的理由是 。
③ 已知Zn(l)=Zn(g) ΔH =" +116" KJ/mol 。若SiCl4的轉化率均為90%,每投入1mol SiCl4,“反應3”比“反應2”多放出_____kJ的熱量。
(5)用硅制作太陽能電池時,為減弱光在硅表面的反射,采用化學腐蝕法在其表面形成粗糙的多孔硅層。腐蝕劑常用稀HNO3和HF的混合液。硅表面首先形成SiO2,最后轉化為H2SiF6。用化學方程式表示SiO2轉化為H2SiF6的過程 。
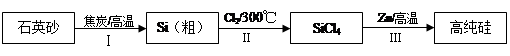
 Si(s) + 2ZnCl2(l) ΔH1 <0
Si(s) + 2ZnCl2(l) ΔH1 <0  Si(s) + 2ZnCl2(g) ΔH2 <0
Si(s) + 2ZnCl2(g) ΔH2 <0  Si(s) + 2ZnCl2(g) ΔH3 <0
Si(s) + 2ZnCl2(g) ΔH3 <0 下列說法正確的是 ![]()
A.太陽能電池可采用二氧化硅材料制作,其應用有利于環保節能
B.我國流通的硬幣材質是金屬單質![]() w.w.w.k.s.5 u.c.o.m
w.w.w.k.s.5 u.c.o.m
C.在廣東沿海打撈上來的明代沉船上存在大量鋁制餐具
D.把氯化物等鹽類撒在雪中,能降低水的熔點,從而有利于除雪![]()
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com