水溶液是中學化學的重點研究對象.
(1)水是極弱的電解質,也是最重要的溶劑.常溫下某電解質溶解在水中后,溶液中的c(H
+)=10
-9mol?L
-1,則該電解質可能是
CD
CD
(填序號).
A. CuSO
4 B. HCl C. Na
2S D.NaOH E.K
2SO
4(2)已知次氯酸是比碳酸還弱的酸,要使新制稀氯水中的c(HClO)增大,可以采取的措施為(至少回答兩種)
再通入氯氣、加入碳酸鹽、加入次氯酸鈉
再通入氯氣、加入碳酸鹽、加入次氯酸鈉
.
(3)常溫下,將pH=3的鹽酸a L分別與下列三種溶液混合,結果溶液均呈中性.
①濃度為1.0×10
-3mol?L
-1的氨水b L;②c(OH
-)=1.0×10
-3mol?L
-1的氨水c L;③c(OH
-)=1.0×10
-3mol?L
-1的氫氧化鋇溶液d L.則a、b、c、d之間的關系是:
b>a=d>c
b>a=d>c
.
(4)強酸制弱酸是水溶液中的重要經驗規律.
①已知HA、H
2B是兩種弱酸,存在以下關系:H
2B(少量)+2A
-=B
2-+2HA,則A
-、B
2-、HB
-三種陰離子結合H
+的難易順序為
A->B2->HB-
A->B2->HB-
.
②某同學將H
2S通入CuSO
4溶液中發現生成黑色沉淀,查閱資料并在老師的指導下寫出了化學方程式:H
2S+CuSO
4=CuS↓+H
2SO
4,但這位同學陷入了困惑:這不成了弱酸制取強酸了嗎?請你幫助解釋
銅離子和硫化氫只所以能生成硫化銅沉淀,是因為硫化銅既難溶于水又難溶于酸
銅離子和硫化氫只所以能生成硫化銅沉淀,是因為硫化銅既難溶于水又難溶于酸
.
(5)已知:H
2A═H
++HA
-、HA
-?H
++A
2-,常溫下,0.1mol?L
-1的NaH A溶液其pH=2,則0.1mol?L
-1的H
2A溶液中氫離子濃度的大小范圍是:
0.1mol/L<c(H+)<0.11mol/L
0.1mol/L<c(H+)<0.11mol/L
;NaHA溶液中各種離子濃度大小關系為
c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
.
(6)己知:Ksp(AgCl)=1.8×10
-10mol?L
-1,向50mL 0.018mol?L
-1的AgNO
3溶液中加入相同體積0.020mol?L
-1的鹽酸,則c(Ag
+)=
1.8×10-7mol/L
1.8×10-7mol/L
,此時所得混合溶液的pH=
2
2
.

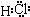
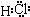
 水的電離平衡曲線如圖所示.
水的電離平衡曲線如圖所示. CO(g)+H2(g)△H=+131kJ?mol-1
CO(g)+H2(g)△H=+131kJ?mol-1 CH3OH(g) 據研究,給合成甲醇反應體系中通入少量CO2有利于維持催化劑Cu2O的量不變,原因是(用化學方程式表示)
CH3OH(g) 據研究,給合成甲醇反應體系中通入少量CO2有利于維持催化劑Cu2O的量不變,原因是(用化學方程式表示) 2Cu+CO2
2Cu+CO2 2Cu+CO2
2Cu+CO2