
題目列表(包括答案和解析)
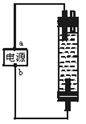
| A.a為正極,b為負極;NaClO和NaCl |
| B.a為負極,b為正極;NaClO和NaCl |
| C.a為陽極,b為陰極;HClO和NaCl |
| D.a為陰極,b為陽極;HClO和NaCl |
|
鋁及鋁合金經過陽極氧化,鋁表面能生成幾十微米厚的氧化鋁膜.某研究性學習小組模擬工業法對鋁片表面進行氧化處理.分別以鉛片、鋁片為電極,以硫酸溶液為電解液,按照如圖所示裝置連接電解池裝置,電解40 min后取出鋁片,用水沖洗,放在水蒸氣中封閉處理20~30 min,即可得到更加致密的氧化膜.下列有關說法正確的是
| |
| [ ] | |
A. |
電解時電子從電源負極→導線→鋁極,鉛極→導線→電源正極 |
B. |
在電解過程中,H+向陽極移動,SO |
C. |
電解過程陽極周圍溶液的pH下降 |
D. |
電解的總反應為2Al+6H+ |
A.銅鋅原電池中銅是負極
B.用電解法精煉粗銅時粗銅作陽極?
C.在鐵上電鍍銅時用銅作陰極?
D.電解稀硫酸時用銅作陽極,陽極產物為氧氣
(12分)Ⅰ.A、B、C、D、E為短周期的五種元素,它們原子序數依次遞增,B是構成有機物的主要元素;A與C可形成10電子化合物W,它可使紫色石蕊試液變藍;D元素的原子最外層電子數是其次外層電子數3倍;E是同周期元素中原子半徑最大的元素;A、B、C、D可形成化合物X,在X晶體中陽離子與陰離子個數比為1∶1;A、D、E可形成化合物Y。A、C、D可形成離子化合物Z。回答下列問題:
⑴Y的電子式: ;W的空間構型: ;
⑵寫出Z的水溶液中各離子濃度由大到小的順序: ;
⑶寫出常溫下X與足量的Y在溶液中反應的離子方程式: ;
⑷寫出由A、B、D形成的化合物在一定條件下制取常見果實催熟劑的化學方程式:
⑸用石墨為電極電解Y的水溶液時,陽極的電極反應式為 ,一段時間后溶液的pH (從“增大”“減小”或“不變”中選填).
Ⅱ.南昌大學研發出一種新型納米鋰電池,已躋身國內領先地位。以下是某種鋰離子的電池反應方程式:(C6Li表示鋰原子嵌入石墨形成的復合材料,LiMO2表示含鋰的過渡金屬氧化物)回答:
⑴鋰電池放電時的負極反應為:C6Li-xe-=C6Li1-x+xLi+,則正極反應為: ;⑵電池放電時若轉移1mol e-,消耗的負極材料 g。
(12分)Ⅰ.A、B、C、D、E為短周期的五種元素,它們原子序數依次遞增,B是構成有機物的主要元素;A與C可形成10電子化合物W,它可使紫色石蕊試液變藍;D元素的原子最外層電子數是其次外層電子數3倍;E是同周期元素中原子半徑最大的元素;A、B、C、D可形成化合物X,在X晶體中陽離子與陰離子個數比為1∶1;A、D、E可形成化合物Y。A、C、D可形成離子化合物Z。回答下列問題:
⑴Y的電子式: ;W的空間構型: ;
;
⑵寫出Z的水溶液中各離子濃度由大到小的順序: ;
⑶寫出常溫下X與足量的Y在溶液中反應的離子方程式: ;
⑷寫出由A、B、D形成的化合物在一定條 件下制取常見果實催熟劑的化學方程式:
件下制取常見果實催熟劑的化學方程式:
⑸用石墨為電極電解Y的水溶液時,陽極的電極反應式為 ,一段時間后溶液的pH (從“增大”“減小”或“不變”中選填).
Ⅱ.南昌大學研發出一種新型納米鋰電池,已躋身國內領先地位。以下是某種鋰離子的電池反應方程式 :
: (C6Li表示鋰原子嵌入石墨形成的復合材料,LiMO2表示含鋰的過渡金屬氧化物)回答:
(C6Li表示鋰原子嵌入石墨形成的復合材料,LiMO2表示含鋰的過渡金屬氧化物)回答:
⑴鋰電池放電時的負極反應為:C6Li -xe-=C6Li1-x+xLi+,則正極反應為: ;⑵電池放電時若轉移1mol e-,消
-xe-=C6Li1-x+xLi+,則正極反應為: ;⑵電池放電時若轉移1mol e-,消 耗的負極材料 g。
耗的負極材料 g。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com