
題目列表(包括答案和解析)
乙醇俗稱酒精,在生活中用途廣泛,工業上可用來制造醋酸、飲料、香精、染料、燃料等,醫療上也常用體積分數為70%~75%的乙醇作消毒劑。某校初三學生在老師的指導下對乙醇的一些性質進行了實驗探究:
【探究活動一】乙醇的化學式是C2H5OH,在NaOH一樣含有“OH”,那么乙醇是不是堿呢?請你試設計一種方案加以驗證.
| 實驗步驟 | 實驗現象 | 實驗結論 |
| | | 乙醇不是堿 |

| 實驗步驟 | 實驗現象 | 實驗結論 |
| | | 小紅同學的想法是正確的,有關實驗現象的反應化學方程式為 |
乙醇俗稱酒精,在生活中用途廣泛,工業上可用來制造醋酸、飲料、香精、染料、燃料等,醫療上也常用體積分數為70%~75%的乙醇作消毒劑。某校初三學生在老師的指導下對乙醇的一些性質進行了實驗探究:
【探究活動一】乙醇的化學式是C2H5OH,在NaOH一樣含有“OH”,那么乙醇是不是堿呢?請你試設計一種方案加以驗證.
|
實驗步驟 |
實驗現象 |
實驗結論 |
|
|
|
乙醇不是堿 |
【探究活動二】根據質量守恒定律,小李同學認為乙醇(C2H5OH)完全燃燒時生成CO2和H2O,如果氧氣不足,乙醇燃燒可生成CO、CO2和H2O。
查閱資料:無水硫酸銅固體遇水由白色變藍色,生成五水硫酸銅(CuSO4•5H2O),一氧化碳具有還原性,高溫或加熱時能將許多金屬氧化物還原金屬單質,因此常用于金屬的冶煉.堿石灰是氧化鈣和氫氧化鈉的混合物,具有很強的吸水性,并能吸收酸性氣體。
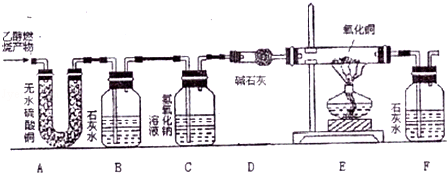
在老師的指導下,同學們用如圖所示的裝置進行實驗,確證乙醇燃燒產物中有CO、CO2和H2O。請回答下列問題:

(1)B裝置的作用是 ;C裝置的作用是 ;D裝置的作用是 。
(2)能確證產物中有H2O的現象是 。實驗時,同學們還觀察到B、F裝置中澄清石灰水變渾濁,C裝置中有氣泡冒出,E裝置中黑色粉末變成紅色,說明該乙醇燃燒產物中有CO、CO2和H2O生成.請寫出E裝置中發生反應的化學方程式: 。
(3)為了保護環境,應在裝置的排氣管口采取的措施是 。
(4)小明同學在反應的過程中發現C裝置內除了氣體通過溶液時產生氣泡之外,沒有明顯變化現象,所以他認為C裝置中沒有發生化學反應,小紅同學認為通過C裝置氣體中仍有部分二氧化碳與氫氧化鈉溶液發生化學反應,為了確證C裝置中是否發生化學變化,他們設計了以下實驗:
|
實驗步驟 |
實驗現象 |
實驗結論 |
|
|
|
小紅同學的想法是正確的,有關實驗現象的反應化學方程式為 |
| 實驗步驟 | 實驗現象 | 實驗結論 |
| | | 乙醇不是堿 |
| 實驗步驟 | 實驗現象 | 實驗結論 |
| | | 小紅同學的想法是正確的,有關實驗現象的反應化學方程式為 |
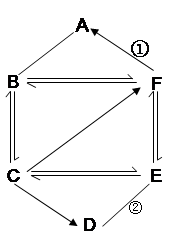
(6分)A~G是初中化學常見的物質,其轉化關系如下圖所示。其中,A是一種紫黑色固體,在加熱的條件下能生成B、D、E三種物質;B和G均是黑色固體,B和F的溶液混合后也能產生D;D和J都是無色無味的氣體,J能用于光合作用和滅火。
(1)寫出下列字母代表的物質的名稱:A ;B 。
(2)G在D中燃燒的實驗現象是___________。文字表達式為 。
(3)L的溶液俗稱為 。寫出J與L反應的文字表達式 。
一、選擇題(共25個小題,每個小題1分,共25分)
題號
1
2
3
4
5
6
7
8
9
10
11
12
13
答案
A
A
B
D
D
C
D
C
B
A
C
A
C
題號
14
15
16
17
18
19
20
21
22
23
24
25
答案
D
B
B
A
B
D
C
C
D
A
D
B
二、填空題(共5個小題,共30分)
26.(共9分,每空1分)
/2009年北京市延慶縣第一學期期末統測初三化學.files/image068.gif) (1)Al O H (2)FeCl3 +4
(1)Al O H (2)FeCl3 +4
(3)B C H2、O2(或Cl2) 2H2+O2 2H2O
27.(共5分,每空1分)
(1) D
(2) 生成物為CO2和H2O,不污染空氣
/2009年北京市延慶縣第一學期期末統測初三化學.files/image069.gif)
(3)2H2O 2H2↑+O2↑ (4) N2 (5)A、B、C
28.(共5分,每空1分)
(1) 氯化鈉(或NaCl) (2) 飽和
(3) 碳酸鈉溶解度隨溫度降低而明顯降低,冬天溫度低,溶解在水中的碳酸鈉就析出,所以冬天可撈堿。 (4) 25 <
29.(共5分)
(1)下降 鎂與稀硫酸反應放熱,致使瓶內氣壓大于外界氣壓(合理即給分)
(2) B、C
(3) ①化學反應常伴有能量變化 ②分子之間有間隔 (2分)(合理即給分)
30.(共6分)
(1)O2 熟石灰
(2)CO2 + Ca(OH)2 == CaCO3↓+ H2O CO + H2O = H2CO3
(3) C、H(或H、Cl) (2分,答對1種元素給1分)
三、實驗題(共3個小題,共19分)
/2009年北京市延慶縣第一學期期末統測初三化學.files/image070.gif) 31.(共8分,每空1分)
31.(共8分,每空1分)
(1) 錐形瓶 (2)A B 2H2O2 2H2O+O2↑
(3) b、c、d、a
(4) CaCO3+2HCl→CaCl2+H2O+CO2↑; C ①③
32.(共5分,每空1分)
密度比空氣密度大、不能燃燒、不能支持燃燒(三點答全得1分)
(1)杯內的氧氣被耗盡,同時又產生了不能燃燒且不能支持燃燒的氣體。(合理即給分)
蠟燭燃燒產生的CO2密度大,會下沉。 高的
(2)①②
33.(共6分,每空1分)
【實驗設計】 氧氣(或O2) ;
增加水中的氧氣含量,供魚苗呼吸
【實驗反思】 氧化鈣與水反應,生成氫氧化鈣。或CaO+H2O→Ca(OH)2
實驗步驟
實驗現象
結論
取反應后所得溶液樣品于試管中,然后通入CO2氣體。
產生白色沉淀(或溶液變渾濁)
2CaO2+2H2O→2Ca(OH)2+O2↑
四、計算題(共2個小題,每小題3分,共6分。最后結果保留一位小數)
34.(共3分,每空1分)
(1) 6∶1 ; 66.7% (2)
35.(共3分)
【解】設:生成次氯酸鈉的質量為X,氫氣的質量為y
MNaCl ==11.7%×
/2009年北京市延慶縣第一學期期末統測初三化學.files/image071.gif) 則:NaCl+H2O
NaClO+H2↑
則:NaCl+H2O
NaClO+H2↑
58.5 74.5 2
/2009年北京市延慶縣第一學期期末統測初三化學.files/image072.gif)
|