
題目列表(包括答案和解析)
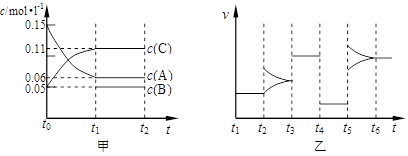
向某密閉容器中加入0.15mol/L A、0.05mol/L C和一定量的B三種氣體。一定條件下發(fā)生反應,各物質濃度隨時間變化如下圖中甲圖所示[t0時c( B)未畫出,t1時增大到0.05mol/L]。乙圖為 t2時刻后改變反應條件,平衡體系中正、逆反應速率隨時間變化的情況。

(1)若t4時改變的條件為減小壓強,則B的起始物質的量濃度為 mol/L;
該反應的平衡常數表達式為K= 。
(2)若t5時改變的條件是升溫,此時v(正) > v(逆),平衡常數K的值將 (選填“增大”、“減小”或“不變”)。
(3)若 t1= 15s,則t0~ t1階段以C 濃度變化表示的平均反應速率為v(C)=
mol/L·s。t3 時改變的某一反應條件可能是 (選填序號)。
a.使用催化劑 b.增大壓強 c.增大反應物濃度 d.降低產物濃度
(4)若A的物質的量減少0.02mol時,容器與外界的熱交換總量為a kJ,寫出該反應的熱化學方程式 。
把大氣中的游離態(tài)的氮轉化為氮的化合物的過程稱為固氮。生物固氮和大氣固氮(閃電時N2轉化為NO)屬于自然固氮,這遠不能滿足人類的需要。工業(yè)固氮(合成氨)是目前人工固氮的主要方法。有關大氣固氮和工業(yè)固氮的平衡常數K值分別如下表一和表二。
表一:N2+ O2  2NO
2NO
| 溫度 | 27℃ | 2000℃ |
| K值 | 3.84×10-31 | 0.1 |
 2NH3
2NH3 | 溫度 | 25℃ | 350℃ | 400℃ | 450℃ |
| K值 | 5×108 | 1.847 | 0.507 | 0.152 |
 2NO是吸熱反應
2NO是吸熱反應
向某密閉容器中加入0.15mol/L A、0.05mol/L C和一定量的B三種氣體。一定條件下發(fā)生反應,各物質濃度隨時間變化如下圖中甲圖所示[t0時c( B)未畫出,t1時增大到0.05mol/L]。乙圖為 t2時刻后改變反應條件,平衡體系中正、逆反應速率隨時間變化的情況。
(1)若t4時改變的條件為減小壓強,則B的起始物質的量濃度為 mol/L;
該反應的平衡常數表達式為K= 。
(2)若t5時改變的條件是升溫,此時v(正) > v(逆),平衡常數K的值將 (選填“增大”、“減小”或“不變”)。
(3)若 t1= 15s,則t0~ t1階段以C 濃度變化表示的平均反應速率為v(C)=
mol/L·s。t3時改變的某一反應條件可能是 (選填序號)。
a.使用催化劑 b.增大壓強 c.增大反應物濃度 d.降低產物濃度
(4)若A的物質的量減少0.02mol時,容器與外界的熱交換總量為a kJ,寫出該反應的熱化學方程式 。
 2NO
2NO | 溫度 | 27℃ | 2000℃ |
| K值 | 3.84×10-31 | 0.1 |
 2NH3
2NH3 | 溫度 | 25℃ | 350℃ | 400℃ | 450℃ |
| K值 | 5×108 | 1.847 | 0.507 | 0.152 |
 2NO是吸熱反應
2NO是吸熱反應
一、選擇題:
1、C 2、A 3、A 4、D 5、B
6-13 DBDDBADB
14.B15.AC16.AD17.C18.A19.C20.ABD21.BC
22.(17分)
|