
題目列表(包括答案和解析)
成都七中文藝青年小組進行了關于“活潑金屬與酸反應”的實驗,得出了一些有趣的想法,請你幫助他們,完成一些判斷。將5.4g鋁片投入500mL 0.5 mol·L-1的硫酸溶液中,下圖為反應產氫速率與反應時間的關系圖。
(1)關于圖像的描述不正確的是_③_____(2分)
①a→c段產生氫氣的速率增加較快可能是表面的氧化膜逐漸溶解,加快了反應的速率
②a→c段產生氫氣的速率增加較快可能是該反應放熱,導致溫度升高,加快了反應
③c以后,產生氫氣的速率逐漸下降可能是鋁片趨于消耗完全
(2)書寫O→a段所對應的離子方程式____________________________________(2分)
(3)若其他條件不變,現換用500mL1mol·L-1鹽酸,產生氫氣速率普遍較使用500mL 0.5mol·L-1硫酸的快,可能的原因是_②④_______(2分)
①鹽酸中c(H+)的濃度更大 ②Cl—有催化作用 ③SO42—有催化作用
④SO42—有阻化作用 ⑤Al3+有催化作用
(4)根據所學,若要加快鋁片與硫酸溶液制H2的反應速率,小組成員提出一系列方案,比如:①加入某種催化劑;②滴加少量CuSO4溶液;③將鋁片剪成100條;④增加硫酸的濃度至18mol/L;⑤加入蒸餾水;⑥加入少量KNO3溶液;
⑦_____________。(2分)
其中,你認為不合理的方案有_____________(2分),并請你再補充一種合理方案,填入空白⑦處。
(10分)成都七中文藝青年小組進行了關于“活潑金屬與酸反應”的實驗,得出了一些有趣的想法,請你幫助他們,完成一些判斷。將5.4g鋁片投入500mL 0.5 mol·L-1的硫酸溶液中,下圖為反應產氫速率與反應時間的關系圖。
(1)關于圖像的描述不正確的是_③_____(2分)
①a→c段產生氫氣的速率增加較快可能是表面的氧化膜逐漸溶解,加快了反應的速率
②a→c段產生氫氣的速率增加較快可能是該反應放熱,導致溫度升高,加快了反應
③c以后,產生氫氣的速率逐漸下降可能是鋁片趨于消耗完全
(2)書寫O→a段所對應的離子方程式____________________________________(2分)
(3)若其他條件不變,現換用500mL1mol·L-1鹽酸,產生氫氣速率普遍較使用500mL 0.5mol·L-1硫酸的快,可能的原因是_②④_______(2分)
①鹽酸中c(H+)的濃度更大 ②Cl—有催化作用 ③SO42—有催化作用
④SO42—有阻化作用 ⑤Al3+有催化作用
(4)根據所學,若要加快鋁片與硫酸溶液制H2的反應速率,小組成員提出一系列方案,比如:①加入某種催化劑;②滴加少量CuSO4溶液;③將鋁片剪成100條;④增加硫酸的濃度至18mol/L;⑤加入蒸餾水;⑥加入少量KNO3溶液;⑦_____________。(2分)
其中,你認為不合理的方案有_____________(2分),并請你再補充一種合理方案,填入空白⑦處。
(10分)成都七中文藝青年小組進行了關于“活潑金屬與酸反應”的實驗,得出了一些有趣的想法,請你幫助他們,完成一些判斷。將5.4g鋁片投入500mL 0.5 mol·L-1的硫酸溶液中,下圖為反應產氫速率與反應時間的關系圖。

(1)關于圖像的描述不正確的是______(2分)
①a→c段產生氫氣的速率增加較快可能是表面的氧化膜逐漸溶解,加快了反應的速率
②a→c段產生氫氣的速率增加較快可能是該反應放熱,導致溫度升高,加快了反應
③c以后,產生氫氣的速率逐漸下降可能是鋁片趨于消耗完全
(2)書寫O→a段所對應的離子方程式____________________________________(2分)
(3)若其他條件不變,現換用500mL1mol·L-1鹽酸,產生氫氣速率普遍較使用500mL 0.5mol·L-1硫酸的快,可能的原因是________(2分)
①鹽酸中c(H+)的濃度更大 ②Cl—有催化作用 ③SO42—有催化作用
④SO42—有阻化作用 ⑤Al3+有催化作用
(4)根據所學,若要加快鋁片與硫酸溶液制H2的反應速率,小組成員提出一系列方案,比如:①加入某種催化劑;②滴加少量CuSO4溶液;③將鋁片剪成100條;④增加硫酸的濃度至18mol/L;⑤加入蒸餾水;⑥加入少量KNO3溶液;⑦_____________。(2分)
其中,你認為不合理的方案有_____________(2分),并請你再補充一種合理方案,填入空白⑦處。
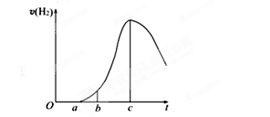
固體粉末X由Fe2O3 、CuO組成,某研究性學習小組選用圖17中裝置(夾持裝置已略去,實驗前均已檢查裝置氣密性)探究X與過量炭粉發(fā)生反應時,除生成![]() 外,是否還有其他氣體產物。
外,是否還有其他氣體產物。
圖17
請回答:
(1)若按甲→丙→丁的順序連接裝置,則____________________(填上圖裝置代號)裝置和試劑需稱量,開始反應,氣體經充分吸收后,分析數據發(fā)現,消耗碳、氧元素的質量大于生成![]() 的質量,可能的原因除產生了
的質量,可能的原因除產生了![]() 外的其他氣體產物,還可能是____ _____________.
外的其他氣體產物,還可能是____ _____________.
(2)為使實驗測得的數據更能準確說明問題,一些同學按乙→丁→戊的順序連接裝置進行實驗,并且加熱前先通一會氣體M,停止加熱后再通一會兒該氣體。
①氣體M可能是____________ (填字母)。
a.![]() b.
b.![]() c.
c.![]() d.CO e.
d.CO e.![]()
②停止加熱后再通一會氣體M的原因是_________________________________________。
(3)以上兩套裝置均存在的同樣的明顯缺陷是____________________________________。
(4)該小組同學設計實驗(如圖18)將X進行轉化(每一步均反應完全):
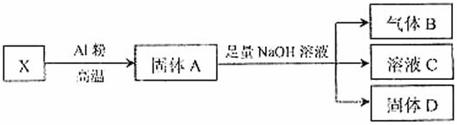
圖18
①生成氣體B的化學方程式是___________________________________________ 。
②將固體D投入過量稀硫酸并充分反應后,過濾,再向濾液加入雙氧水,得黃色溶液。
寫出當加入雙氧水時溶液中發(fā)生反應的離子方程式:
____________________________________________________________。
③若已知固體X的質量為7.2g反應中AI粉的質量是2.7g,氣體B在標準狀況下的體積為672ml,則固體D的質量是_________ g.
一、選擇題(48分)
1.B 2.B 3.D 4.C 5.A 6.A D 7.B C 8.A B
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image211.jpg) 二、實驗題(18分)
二、實驗題(18分)
9.(1)(6分)
10.紅光(4分)
11.(1)R2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image068.gif) (或C)(2分) (2)如圖(2分)
(或C)(2分) (2)如圖(2分)
(3)896.42008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image214.gif) (2分) 偏大 (2分)
(2分) 偏大 (2分)
三、計算題(54分)
12.(16分)解:小車固定在地面時,設物體與小車間摩擦力為f,由動能定理
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image216.gif) (1)
(1)
把小車放在光滑水平地面上時,小物體與小車間摩擦力仍為f.設小物體相對小車滑行距離為L時,跟小車相對靜止(未能滑離小車)共同速度為V,由動量守恒定律
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image218.gif) (2)
(2)
設這過程小車向前滑行距離為S。由動能定理
對小車有2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image220.gif) (3)
(3)
對小物體有2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image222.gif)
由(2)(3)(4)解出2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image224.gif) (5)
(5)
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image226.gif) 且
且2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image228.gif) (6)
(6)
比較(5)(6)解出2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image230.gif) ,只要
,只要2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image232.gif) 小物體就能滑離小車
小物體就能滑離小車
13.(18分) 解:(1)2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image234.gif)
(2)剛釋放2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image236.gif) 棒時,
棒時,2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image238.gif)
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image236.gif) 棒受到安培力為:
棒受到安培力為:2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image241.gif)
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image236.gif) 棒受到的種力為:
棒受到的種力為:2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image244.gif)
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image246.gif) 棒沿導軌向下加速滑動,既abcd閉合回路的
棒沿導軌向下加速滑動,既abcd閉合回路的2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image248.gif) 增大;
增大;
電流也將增大,所以最小電流為:2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image250.gif) ;
;
當2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image236.gif) 棒的速度達到最大時,回路的電流最大,此時
棒的速度達到最大時,回路的電流最大,此時2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image236.gif) 棒的加速度為零。
棒的加速度為零。
由2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image254.gif) 得
得2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image256.gif)
(3)由:2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image258.gif) 得:
得:2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image260.gif)
14.解:(20分)(1)帶電粒子從原點射出進入勻強磁場,在垂直于磁場的2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image262.gif) 平面內做勻速圓周運動由左手定則判斷磁場的方向垂直于
平面內做勻速圓周運動由左手定則判斷磁場的方向垂直于2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image262.gif) 平面指向紙外。從粒子進入電場受力作用而速度偏高分析判斷:電場強度方向是平行x軸,沿
平面指向紙外。從粒子進入電場受力作用而速度偏高分析判斷:電場強度方向是平行x軸,沿2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image265.gif) 軸負方向。
軸負方向。
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image267.jpg)
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image269.gif) 距離應是帶電粒子在勻強磁場中作圓周運動的軌跡直徑,從
距離應是帶電粒子在勻強磁場中作圓周運動的軌跡直徑,從2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image094.gif) 到
到2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image034.gif) 經理半個周期,即:
經理半個周期,即:
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image273.gif) ①
①
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image275.gif) ②
②
解出2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image277.gif) ③
③
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image279.gif)
(2)帶電粒子以2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image281.gif) (大小等于
(大小等于2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image077.gif) 的大小)垂直射入勻強電場,受電場力作用而做曲線運動,(相當于平拋運動軌跡)
的大小)垂直射入勻強電場,受電場力作用而做曲線運動,(相當于平拋運動軌跡)
設勻強電場的場強大小為E,粒子射出電場的速度為2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image284.gif) ,
,
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image286.gif) ⑤
⑤
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image288.gif) ⑥
⑥
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image290.gif) ⑦
⑦
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image292.gif) ⑧
⑧
射出電場時2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image284.gif) 與
與2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image295.gif) 軸夾角120°,即與
軸夾角120°,即與2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image297.gif) 夾角60°
夾角60°
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image299.gif) ⑨
⑨
由⑤、⑥、⑦、⑧、⑨解出 2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image301.gif)
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image303.gif) ①―⑨式子每個2分 結果2分
①―⑨式子每個2分 結果2分
(化學部分)參考答案
1.A 2.B 3.D 4.B 5.C 6.C
7.(14分)
(1)2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image305.jpg)
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image307.gif)
(2)第三周期第ⅥA族
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image309.gif)
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image311.gif)
(3)2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image313.gif)
8.(18分)
(1)2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image315.gif)
(2)羥基 取代反應 消去反應
(3)1:1:3
(4)2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image317.jpg)
(5)2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image318.jpg)
(生物部分)參考答案
一、單項選擇題(每題6分,共36分)
1.A 2.C 3.D 4.C 5.B 6.C
二、非選擇題(除標注外,每空2分,共44分)
7.(1)細菌 營養(yǎng)物質消耗盡了
(2) 圖畫準確 (2分)。 有a、b標示(1分) 捕食
2008―2009學年度第二學期高三總復習質量調查(一)理科綜合.files/image320.jpg)
(3)細菌 小球藻 細菌可以為小球藻提供礦質營養(yǎng)與二氧化碳、小球海可以為細菌提供有機營養(yǎng)與氧氣
8(一) (1)光反應 色素的數量 二氧化碳含量、溫度等
(2) 酶的活性 (3)三碳化合物
(4)
適當降低室內溫度 因為在該光照強度以下,
低溫時(
8(二)(1) ①切成大小相等的若干小塊
②分別加入10ml (等量)過氧化氫溶液
③再分別加入2,4,6個土豆小塊
④定時觀察記錄針筒內體積的變化。
(2)溫度 土豆的新鮮程度 注射器的密封性 注射器針筒與活塞之間的摩擦力等(任答兩項,其他答案合理也可)
(3)延長、縮短
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com