
題目列表(包括答案和解析)
下圖是幾種鹽的溶解度曲線,根據曲線判斷下列說法正確的是

A.20℃時,硝酸鉀飽和溶液的質量分數是31.6%
B.30℃時,將35 g硝酸鉀和35g食鹽同時溶于l00g水中,蒸發時先析出的是氯化鈉
C.40℃時,35 g食鹽溶于l00 g水中,降溫至0C時,可析出氯化鈉晶體
D.60℃時,200 g水中溶解80 g硫酸銅達飽和,當降溫至30℃時,可析出30g硫酸銅晶體
下圖是幾種鹽的溶解度曲線,根據曲線判斷下列說法正確的是
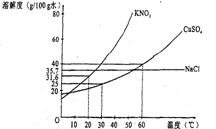
A.20℃時,硝酸鉀飽和溶液的質量分數是31.6%
B.30℃時,將35 g硝酸鉀和35g食鹽同時溶于l00g水中,蒸發時先析出的是氯化鈉
C.40℃時,35 g食鹽溶于l00 g水中,降溫至0C時,可析出氯化鈉晶體
D.60℃時,200 g水中溶解80 g硫酸銅達飽和,當降溫至30℃時,可析出30g硫酸銅晶體
下圖是幾種鹽的溶解度曲線,根據曲線判斷下列說法正確的是
A.20℃時,硝酸鉀飽和溶液的質量分數是31.6%
B.30℃時,將35 g硝酸鉀和35g食鹽同時溶于l00g水中,蒸發時先析出的是氯化鈉
C.40℃時,35 g食鹽溶于l00 g水中,降溫至0C時,可析出氯化鈉晶體
D.60℃時,200 g水中溶解80 g硫酸銅達飽和,當降溫至30℃時,可析出30g硫酸銅晶體
下面是某化學學習小組的同學進行研究性學習的過程,請你參與并協助他們完成相關學習任務。
I.課本介紹了乙醇氧化的實驗:把一端彎成螺旋狀的銅絲放在酒精燈外焰加熱,待銅絲表面變黑后立即把它插入盛有約2 mL乙醇的試管里,反復操作幾次。注意聞生成物的氣味,并觀察銅絲表面的變化。
(1)小趙同學用化學方法替代“聞生成物的氣味”來說明生成物的出現,該化學方法中所另加的試劑及出現的主要現象是: 。(用所學的知識回答)。
(2)小趙同學在探究“聞生成物的氣味”的替代方法時,偶然發現向溴水中加入足量的乙醛溶液,可以看到溴水褪色。該同學為解釋上述現象,提出三種猜想:(注:褪色原因只有一種)
①溴與乙醛發生取代反應;② ;③由于醛基具有還原性,溴將乙醛氧化為乙酸。
為探究哪種猜想正確,小李同學提出了
如下兩種實驗方案:
方案一:用pH試紙檢測溴水褪色后溶液的酸堿性;
方案二:測定反應前溴水中Br2的物質的量和反應后溶液中Br—離子的物質的量。
(3)根據方案一,若 ,則猜想②不成立。
(4)小李同學認為:假設測得反應前溴水中Br2的物質的量為amol,若測得反應后n(Br—)= mol,則說明溴與乙醛發生取代反應。
(5)小吳同學設計如下實驗方案:①按物質的量之比為1:5配制KBrO3—KBr溶液,加合適的適量的酸,完全反應并稀至1L,生成0.5molBr2。②取上述溶液10mL加入足量乙醛溶液,使之褪色,然后將所得溶液稀釋為100mL,準確量取其中10mL。③加入過量的AgNO3溶液,過濾、洗滌、干燥后稱量得到淡黃色固體0.188g。若已知CH3COOAg易溶于水。
試通過計算判斷:溴與乙醛發生反應的化學方程式為 ;
小張同學認為合適的酸既不是硫酸也不是鹽酸,這是為什么? 。
Ⅱ.小錢同學利用下圖裝置進行乙醇的催化氧化實驗并制取乙醛(試管丙中用水吸收產物),圖中鐵架臺等裝置已略去。實驗時,先加熱玻璃管中的銅絲,約lmin后鼓入空氣。

請填寫下列空白:
(1)乙醇發生催化氧化的化學方程式為 。
(2)實驗時,小錢同學將甲裝置浸在70℃~80℃的水浴中,目的是 _。
小孫同學認為:由于小錢同學裝置設計上的缺陷,實驗進行時可能會 ____________。
(3)反應發生后,移去酒精燈,利用反應自身放出的熱量可維持反應繼續進行。進一步探究表明,鼓氣速度與反應體系的溫度關系曲線如圖所示。

請你解釋鼓氣速度過快,反應體系溫度反而下降的原因是: 。
你認為該實驗中“鼓氣速度”這一變量可用 來計量。
下面是某化學學習小組的同學進行研究性學習的過程,請你參與并協助他們完成相關學習任務。
I.課本介紹了乙醇氧化的實驗:把一端彎成螺旋狀的銅絲放在酒精燈外焰加熱,待銅絲表面變黑后立即把它插入盛有約2 mL乙醇的試管里,反復操作幾次。注意聞生成物的氣味,并觀察銅絲表面的變化。
(1)小趙同學用化學方法替代“聞生成物的氣味”來說明生成物的出現,該化學方法中所另加的試劑及出現的主要現象是: 。(用所學的知識回答)。
(2)小趙同學在探究“聞生成物的氣味”的替代方法時,偶然發現向溴水中加入足量的乙醛溶液,可以看到溴水褪色。該同學為解釋上述現象,提出三種猜想:(注:褪色原因只有一種)
①溴與乙醛發生取代反應;② ;③由于醛基具有還原性,溴將乙醛氧化為乙酸。
為探究哪種猜想正確,小李同學提出了
如下兩種實驗方案:
方案一:用pH試紙檢測溴水褪色后溶液的酸堿性;
方案二:測定反應前溴水中Br2的物質的量和反應后溶液中Br—離子的物質的量。
(3)根據方案一,若 ,則猜想②不成立。
(4)小李同學認為:假設測得反應前溴水中Br2的物質的量為amol,若測得反應后n(Br—)= mol,則說明溴與乙醛發生取代反應。
(5)小吳同學設計如下實驗方案:①按物質的量之比為1:5配制KBrO3—KBr溶液,加合適的適量的酸,完全反應并稀至1L,生成0.5molBr2。②取上述溶液10mL加入足量乙醛溶液,使之褪色,然后將所得溶液稀釋為100mL,準確量取其中10mL。③加入過量的AgNO3溶液,過濾、洗滌、干燥后稱量得到淡黃色固體0.188g。若已知CH3COOAg易溶于水。
試通過計算判斷:溴與乙醛發生反應的化學方程式為 ;
小張同學認為合適的酸既不是硫酸也不是鹽酸,這是為什么? 。
Ⅱ.小錢同學利用下圖裝置進行乙醇的催化氧化實驗并制取乙醛(試管丙中用水吸收產物),圖中鐵架臺等裝置已略去。實驗時,先加熱玻璃管中的銅絲,約lmin后鼓入空氣。
請填寫下列空白:
(1)乙醇發生催化氧化的化學方程式為 。
(2)實驗時,小錢同學將甲裝置浸在70℃~80℃的水浴中,目的是 _。
小孫同學認為:由于小錢同學裝置設計上的缺陷,實驗進行時可能會 ____________。
(3)反應發生后,移去酒精燈,利用反應自身放出的熱量可維持反應繼續進行。進一步探究表明,鼓氣速度與反應體系的溫度關系曲線如圖所示。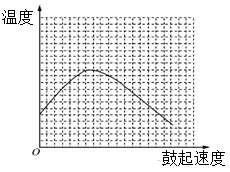
請你解釋鼓氣速度過快,反應體系溫度反而下降的原因是: 。
你認為該實驗中“鼓氣速度”這一變量可用 來計量。
1.D 2.B 3.B 4.D 5.A 6.AD 7.D 8.AD 9.A 10.AC 11.AC
12.D 13.BC 14.D 15.C 16.D 17.A 18.B 19.A 20.A 21.C 22.D
23.(1)CuS、S (2)6∶1∶4
(3)

24.(1)D (2)> (3)B
25.解析:(1)
(2)因 中的
中的 ,
, 中的
中的 ,故依電子得失守恒有(x+1)×25.00×0.1000=5×30.00×0.0500,解之,x+2,即
,故依電子得失守恒有(x+1)×25.00×0.1000=5×30.00×0.0500,解之,x+2,即 被氧化成+2價氮的氧化物NO.又因V×C×2=30.00×0.0500×5,故
被氧化成+2價氮的氧化物NO.又因V×C×2=30.00×0.0500×5,故 .依題意知,
.依題意知,


 .所以
.所以 與
與 反應的方程式為
反應的方程式為

 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
26.解析:這是一道天平平衡問題的計算.兩個燒杯的質量相等.兩個燒杯里鹽酸溶液的質量相等.因此論證天平兩個燒杯內反應體系質量改變量相等是解決本題的關鍵.由題意可知:
 溶液增重
溶液增重
100 56
a
 溶液增重
溶液增重
84 40
x 40x/84
當0.3 mol HCl與 恰好完全反應時,消耗
恰好完全反應時,消耗 的質量為:
的質量為: 時;0.3 mol HCl與
時;0.3 mol HCl與 恰好完全反應,消耗
恰好完全反應,消耗 的質量為:0.3×84=
的質量為:0.3×84=
(1)a≤ 、
、 均過量,天平保持平衡的條件是:
均過量,天平保持平衡的條件是:
 x=
x=
(2)a> 不足,且對于
不足,且對于 恰好完全反應時,加入
恰好完全反應時,加入 的燒杯內反應體系的增重量為a-0.15×44,而加入
的燒杯內反應體系的增重量為a-0.15×44,而加入 的燒杯內反應體系的增重量為0.3×40.則天平保持平衡的條件是:
的燒杯內反應體系的增重量為0.3×40.則天平保持平衡的條件是:
a-0.15×44=0.3×40 a=18.6
因此,18.6≥a>15時,天平保持平衡的條件是:
 x=2,
x=2,
(3)當a>18.6時,天平保持平衡的條件是:a-0.15×44=x-0.3×44
x=a+6.6
因為燒杯中無固體剩余,說明a≤15. 、
、 的摩爾質量相當,當等質量的
的摩爾質量相當,當等質量的 、
、 與酸完全反應時,生成
與酸完全反應時,生成 質量相等.所以天平保持平衡時:x=a≤15
質量相等.所以天平保持平衡時:x=a≤15
27.解析:題中涉及化學反應如下: w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
 ①
①
 ②
②
 ③
③
(1)當剩余固體為 ,排出氣體為
,排出氣體為 、
、 時,因為沒有NaOH生成,水未與
時,因為沒有NaOH生成,水未與 反應.將方程式①×2+②得:
反應.將方程式①×2+②得:

由方程式可知: .
.
(2)當剩余固體為 、NaOH,排出氣體為
、NaOH,排出氣體為 、
、 時,由于有NaOH生成,所以有水與
時,由于有NaOH生成,所以有水與 反應.假設反應后無
反應.假設反應后無 生成,將方程式①×2+②+③得:
生成,將方程式①×2+②+③得:

由方程式可知此時 .因為有水生成,所以
.因為有水生成,所以
(3)當 時,由2討論可知:剩余固體為
時,由2討論可知:剩余固體為 、NaOH、
、NaOH、 ;排出氣體為
;排出氣體為 .
.
(4)當排出的 和
和 為等物質的量時,依方程式討論有:
為等物質的量時,依方程式討論有:

2b b b

b b 
設反應的 的物質的量為x
的物質的量為x

x x 
依題意有:

所以,反應中消耗 的物質的量為:
的物質的量為: ,用去
,用去 的物質的量為:
的物質的量為:
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
所以,
28.(1)0~50℃時, 不發生分解,固體物質質量不變
不發生分解,固體物質質量不變
(2)50℃~ 分解的結果,結晶水全部失去
分解的結果,結晶水全部失去

179 143

(3)100℃~ 穩定且不發生分解,故固體質量不變
穩定且不發生分解,故固體質量不變
(4)214℃~ 發生了分解
發生了分解

143 55+16x
0.80 0.40
x≈1 y=1.5,
故反應方程式為
(5)280℃~ 反應生成高價態氧化物
反應生成高價態氧化物
 方程式為
方程式為

29.解:假設反應后的混合物標況下仍為氣體且體積為 ,由
,由 ,得
,得
 ,可見反應前后物質的量不變,設烷烴為
,可見反應前后物質的量不變,設烷烴為 ,體積為x,則CO為
,體積為x,則CO為
由 體積減少
體積減少

 體積增加
體積增加
 nL (n+1)L
nL (n+1)L 
x

據題意得: nx=
nx=
討論:(1)n=l時,x=
(2)n=2時,
(3)n=3時,
(4)n=4時,
(5)n≥5時,常溫下烷烴不是氣態,所以,烷烴可能是 占50%或是:
占50%或是: 占33.3%或:
占33.3%或: 占25%
占25% w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
30.(1)

2 mol 2 mol 2 mol 2 mol
溶液中剩余的水的質量為:
析出小蘇打的質量為:
(2) 和
和
當降溫至 的質量為:
的質量為:

析出 的質量為:
的質量為:
 共析出晶體的質量為:
共析出晶體的質量為: www.ks5u.com
www.ks5u.com
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com