
題目列表(包括答案和解析)
 Mn、Fe均為第四周期過渡元素,兩元素的部分電離能數據如下表:
Mn、Fe均為第四周期過渡元素,兩元素的部分電離能數據如下表:| 元素 | Mn | Fe | |
電離能(kJ/mol) |
I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
Mn、Fe均為第四周期過渡元素,兩元素的部分電離能數據列于下表:
| 元 素 | Mn | Fe | |
| 電離能 /kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 |
回答下列問題:
⑴亞鐵離子價電子層的電子排布式為
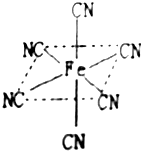
⑵ Fe原子或離子外圍有較多能量相近的空軌道而能與一些分子或離子形成配合物。
①與Fe原子或離子形成配合物的分子或離子應具備的結構特征是 ;
② 六氰合亞鐵離子(Fe(CN)64-)中的配體CN-中C原子的雜化軌道類型是 ,寫出一種與CN-互為等電子體的單質分子的電子式 ;
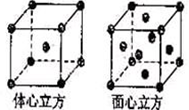
⑶ 金屬鐵的晶體在不同溫度下有兩種堆積方式,晶胞分別如右圖所示。體心立方晶胞和面心立方晶胞中實際含有的Fe原子個數之比為 。
(10分)Mn、Fe均為第四周期過渡元素,兩元素的部分電離能(I)數據列于下表:
| 元素 | 25Mn | 26Fe | |
| 電離能/kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
Mn、Fe均為第四周期過渡元素,兩元素的部分電離能數據列于下表:
| 元 素 | Mn | Fe | |
| 電離能 /kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
 與Fe原子或離子形成配合物的分子或離子應具備的結構特征是 ;
與Fe原子或離子形成配合物的分子或離子應具備的結構特征是 ;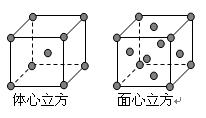
Mn、Fe均為第四周期過渡元素,兩元素的部分電離能數據列于下表:

回答下列問題:
(1)Mn元素價電子的電子排布式為??????????????????????? ,比較兩元素的I2、I3可知,氣態Mn2+再失去一個電子比氣態Fen再失去一個電子難。其原因是??????????????? 。
(2)Fe原子或離子外圍有較多能量相近的空軌道能與一些分子或離子形成配合物。
①與Fe原子或離子形成配合物的分子或離子應具備的結構特征是???????????? 。
②絡離子[Fe(CN)6]4-的配體CN-中C原子的雜化軌道類型是??????????? ,寫出一種與 CN-互為等電子體的單質分子的電子式?????????????????????????? 。
(3)三氯化鐵常溫下為固體,熔點282℃,沸點315℃,在300℃以上升華。易溶于水,也易溶于乙醚、丙酮等有機溶劑。據此判斷三氯化鐵的晶體類型為???????????????? 。
(4)金屬鐵晶體在不同的溫度下有兩種堆積方式,如圖所示。體心立方晶胞和面心立方晶胞中實際含有的Fe原子個數之比為????????????? 。

題號
1
2
3
4
5
6
7
8
9
10
11
12
13
14
答案
B
D
A
A
C
D
B
D
B
B
AC
AD
BC
C
15.(10分,每空2分)
(1)過濾(洗滌) ; 蒸發濃縮、冷卻結晶,過濾
(2)連接好裝置,從漏斗向量氣筒內注入一定量的水,移動漏斗使左、右兩側形成液面高度差。靜置后,液面高度不再變化,即表明氣密性良好。(其他合理方法均給分)
16.(8分)(1)Al
(2)1.204×1024(或2NA)(2分)
(3)4NH3+5O2 4NO+6H2O(2分)
4NO+6H2O(2分)
(4)AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-(2分);
 17.(10分,每空2分) (1)HC2O4-+ OH―= C2O42-+ H2O (2)>
17.(10分,每空2分) (1)HC2O4-+ OH―= C2O42-+ H2O (2)>
(3)H2C2O4 CO↑+CO2↑+H2O
(4)溫度過低反應速率緩慢;溫度過高時,H2C2O4在酸性溶液中會部分分解。(每個點1分 共2分)
(5)C
18.(10分)(1)保護臭氧層(1分)
(3)A(2分)
②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=-49.47kJ•mol-1(2分)
CH3OH(g)+H2O(g) ΔH=-49.47kJ•mol-1(2分)

 (5)B或D(B、D都選給分)(1分)
(5)B或D(B、D都選給分)(1分)
19.(12分,每空2分)
 (1)反應①:加成反應;反應④:取代反應(2) A:CH3CCN; G:
(1)反應①:加成反應;反應④:取代反應(2) A:CH3CCN; G:
(3)B→C;CH3CCOOH CH2=CCOOH+H2O
 |
 |
||||
 |
|||||

|