
題目列表(包括答案和解析)
| A.再通入少量氯氣,[H+]/[ClO-]減小 |
| B.通入少量SO2,溶液漂白性增強 |
| C.加入少量NaOH,一定有[Na+]=[Cl-]+[ClO-] |
| D.加入少量水,水的電離平衡正反應方向移動 |
氯氣溶于水達到平衡后,若其它條件不變,只改變某一條件,下列敘述正確的是
A. 再通入少量氯氣,[H+]/[ClO-]減少
B. 加入少量水,水的電離平衡向正反應方向移動
C. 通入少量SO2,溶液漂白性增強
D. 加入少量固體NaOH,一定有[Na+]=[Cl-]+[ClO-]
(15分)納米級Cu2 O 粉末,由于量子尺寸效應,其具有特殊的光學、電學及光電化學性質,在太陽電池、傳感器、超導體、制氫和電致變色、環境中處理有機污染物等方面有著潛在的應用。
Ⅰ.納米氧化亞銅的制備
(1)四種制取Cu2O的方法如下:
①火法還原。用炭粉在高溫條件下還原CuO;
②最新實驗研究用肼(N2H4)還原新制Cu(OH)2可制備納米級Cu2O,同時放出N2。
已知:N2H4(l)+O2(g) N2(g)+2H2O(l)
△H=-a
kJ/mol
N2(g)+2H2O(l)
△H=-a
kJ/mol
Cu(OH)2(s) CuO(s)+H2O(l) △H=b kJ/mol
CuO(s)+H2O(l) △H=b kJ/mol
4CuO(s) 2Cu2O(s)+O2(g)
△H=c
kJ/mol
2Cu2O(s)+O2(g)
△H=c
kJ/mol
則該方法制備Cu2O的熱化學方程式為 。
③工業中主要采用電解法:用銅和鈦作電極,電解氯化鈉和氫氧化鈉的混合溶液,電解總方程式為:2Cu+H2O Cu2O+H2↑,則陽極反應式為:
。
Cu2O+H2↑,則陽極反應式為:
。
④還可采用Na2SO3還原CuSO4法:將Na2SO3 和CuSO4加入溶解槽中,制成一定濃度的溶液,通入蒸氣加熱,于100℃~104℃間反應即可制得。寫出該反應的化學方程式: 。
Ⅱ.納米氧化亞銅的應用
(2)用制得的Cu2O進行催化分解水的實驗
①一定溫度下,在2 L密閉容器中加入納米級Cu2O并通入10. 0 mol水蒸氣,發生反應:
2H2O(g)  2H2(g)+O2(g)
△H=+484 kJ·mol-1
2H2(g)+O2(g)
△H=+484 kJ·mol-1
T1溫度下不同時段產生O2的量見下表:
|
時間/min |
20 |
40 |
60 |
80 |
|
n(O2)/mol |
1.0 |
1.6 |
2.0 |
2.0 |
前20 min的反應速率 v(H2O)= ;該該溫度下,反應的平衡常數的表達式K= ;若T2溫度下K=0.4,T1 T2(填>、<、=)
②右圖表示在t1時刻達到平衡后,只改變一個條件又達到平衡的不同時段內,H2的濃度隨時間變化的情況,則t1時平衡的移動方向為 ,t2時改變的條件可能為 ;若以K1、K2、K3分別表示t1時刻起改變條件的三個時間段內的平衡常數,t3時刻沒有加入或減少體系中的任何物質,則K1、K2、K3的關系為 ;

③用以上四種方法制得的Cu2O在其它條件相同下分別對水催化分解,產生氫氣的速率v隨時間t變化如圖所示。下列敘述正確的是 。

A.方法③、④制得的Cu2O催化效率相對較高
B.方法④制得的Cu2O作催化劑時,水的平衡轉化率最高
C.催化效果與Cu2O顆粒的粗細、表面活性等有
D.Cu2O催化水分解時,需要適宜的溫度
 N2(g)+2H2O(l) △H="-a" kJ/mol
N2(g)+2H2O(l) △H="-a" kJ/mol CuO(s)+H2O(l) △H="b" kJ/mol
CuO(s)+H2O(l) △H="b" kJ/mol 2Cu2O(s)+O2(g) △H="c" kJ/mol
2Cu2O(s)+O2(g) △H="c" kJ/mol Cu2O+H2↑,則陽極反應式為: 。
Cu2O+H2↑,則陽極反應式為: 。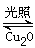 2H2(g)+O2(g) △H=+484 kJ·mol-1
2H2(g)+O2(g) △H=+484 kJ·mol-1| 時間/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 1.0 | 1.6 | 2.0 | 2.0 |


湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com