
題目列表(包括答案和解析)
| 實驗步驟 | 預期現象和結論 |
| 步驟1:取適量試劑于潔凈燒杯中,加入足量蒸餾水,充分攪拌,靜置,過濾,得濾液和沉淀. | |
| 步驟2:取適量濾液于試管中,滴加稀硫酸. | |
| 步驟3:取適量步驟1中的沉淀于是試管中, 取適量步驟1中的沉淀于是試管中,滴加稀鹽酸,用帶塞導氣管塞緊試管,把導氣管插入裝有澄清石灰水的燒杯中 取適量步驟1中的沉淀于是試管中,滴加稀鹽酸,用帶塞導氣管塞緊試管,把導氣管插入裝有澄清石灰水的燒杯中 |
|
| 步驟4: |
0.25L×
| ||
| wg |
0.25L×
| ||
| wg |
某同學進行試驗探究時,欲配制1.0molL-1Ba(OH)2溶液,但只找到在空氣中暴露已久的Ba(OH)2·8H2O試劑(化學式量:315)。在室溫下配制溶液時發現所取試劑在水中僅部分溶解,燒杯中存在大量未溶物。
為探究原因,該同學查得Ba(OH)2·8H2O 部分溶解度數據,見下表:
|
溫度 |
283K |
293K |
303K |
|
溶解度(g/100g H2O) |
2.5 |
3.9 |
5.6 |
(1)燒杯中未溶物僅為BaCO3,理由是 。
(2)假設試劑由大量Ba(OH)2·8H2O和少量BaCO3組成,設計試驗方案,進行成分檢驗,在答題紙上寫出實驗步驟、預期現象和結論。(不考慮結晶水的檢驗;室溫時BaCO3飽和溶液的pH=9.6)
限選試劑及儀器:稀鹽酸、稀硫酸、NaOH溶液、澄清石灰水、pH計、燒杯、試管、帶塞導氣管、滴管
|
實驗步驟 |
預期現象和結論 |
|
步驟1:取適量試劑于潔凈燒杯中,加入足量蒸餾水,充分攪拌,靜置,過濾,得濾液和沉淀。 |
###### |
|
步驟2:取適量濾液于試管中,滴加稀硫酸。 |
_______________________ |
|
步驟3:取適量步驟1中的沉淀于試管中, ,連接帶塞導氣管將產生的氣體導入澄清石灰水中。 |
_______________________ ______________________ |
|
步驟4:取步驟1中的濾液于燒杯中,______________________________ |
_______________________,說明該試劑中含有Ba(OH)2。 |
(3)將試劑初步提純后,準確測定其中Ba(OH)2·8H2O的含量。
實驗如下:①配制250 mL 約0.1mol·L-1Ba(OH)2·8H2O溶液:準確稱取w克試樣,置于燒杯中,加適量蒸餾水,攪拌,將溶液轉入 ,洗滌,定容,搖勻.
②滴定:準確量取25.00ml所配制Ba(OH)2溶液于錐形瓶中,滴加指示劑,將 (填“0.020”、“0.05”、“0.1980”或“1.5”)molL-1鹽酸裝入50ml酸式滴定管,滴定至終點,記錄數據。重復滴定2次。平均消耗鹽酸Vml。
(4)室溫下, (填“能”或“不能”) 配制1.0 mol·L-1Ba(OH)2溶液,說明理由________________________________________________________________________________________.
(12分)某同學進行實驗研究時,欲配制1.0 mol·L-1 Ba(OH)2溶液,但只找到在空氣中暴露已久的Ba(OH)2·8H2O試劑(化學式量:315)。在室溫下配制溶液時發現所取試劑在水中僅部分溶解,燒杯中存在大量未溶物。為探究其原因,該同學查得Ba(OH)2·8H2O在283 K、293 K和303 K時的溶解度(g/100 g H2O)分別為2.5、3.9和5.6。
(1)假設試劑由大量Ba(OH)2·8H2O和少量BaCO3組成。設計實驗方案,進行成分檢驗。寫出實驗步驟、預期現象和結論。(不考慮結晶水的檢驗;室溫時BaCO3飽和溶液的pH=9.6)
限選試劑及儀器:稀鹽酸、稀硫酸、NaOH溶液、澄清石灰水、pH計、燒杯、試管、帶塞導氣管、滴管
| 實驗步驟 | 預期現象和結論 |
| 步驟1:取適量試劑于潔凈燒杯中,加入足量蒸餾水,充分攪拌,靜置,過濾,得濾液和沉淀。 |
|
| 步驟2:取適量濾液于試管中,滴加稀硫酸。 |
|
| 步驟3:取適量步驟1中的沉淀于試管中,________。 |
|
| 步驟4: |
|
(2)將試劑初步提純后,準確測定其中Ba(OH)2·8H2O的含量。實驗如下:
①配制250 mL約0.1 mol·L-1 Ba(OH)2溶液:準確稱取w克試樣,置于燒杯中,加適量蒸餾水,________,將溶液轉入________中,洗滌,定容,搖勻。
②滴定:準確量取25.00 mL所配Ba(OH)2溶液于錐形瓶中,滴加指示劑,將______(填“0.020”、“0.05”、“0.1980”或“1.5”)mol·L-1鹽酸裝入50 mL酸式滴定管,滴定至終點,記錄數據。重復滴定2次。平均消耗鹽酸V mL。
③計算Ba(OH)2·8H2O的質量分數=________(只列出算式,不做運算)。
(3)室溫下,_______(填“能”或“不能”) 配制1.0 mol·L-1 Ba(OH)2溶液。
(12分)某同學進行實驗研究時,欲配制1.0 mol·L-1 Ba(OH)2溶液,但只找到在空氣中暴露已久的Ba(OH)2·8H2O試劑(化學式量:315)。在室溫下配制溶液時發現所取試劑在水中僅部分溶解,燒杯中存在大量未溶物。為探究其原因,該同學查得Ba(OH)2·8H2O在283 K、293 K和303 K時的溶解度(g/100 g H2O)分別為2.5、3.9和5.6。
(1)假設試劑由大量Ba(OH)2·8H2O和少量BaCO3組成。設計實驗方案,進行成分檢驗。寫出實驗步驟、預期現象和結論。(不考慮結晶水的檢驗;室溫時BaCO3飽和溶液的pH=9.6)
限選試劑及儀器:稀鹽酸、稀硫酸、NaOH溶液、澄清石灰水、pH計、燒杯、試管、帶塞導氣管、滴管
|
實驗步驟 |
預期現象和結論 |
|
步驟1:取適量試劑于潔凈燒杯中,加入足量蒸餾水,充分攪拌,靜置,過濾,得濾液和沉淀。 |
|
|
步驟2:取適量濾液于試管中,滴加稀硫酸。 |
|
|
步驟3:取適量步驟1中的沉淀于試管中,________。 |
|
|
步驟4: |
|
(2)將試劑初步提純后,準確測定其中Ba(OH)2·8H2O的含量。實驗如下:
①配制250 mL約0.1 mol·L-1 Ba(OH)2溶液:準確稱取w克試樣,置于燒杯中,加適量蒸餾水,________,將溶液轉入________中,洗滌,定容,搖勻。
②滴定:準確量取25.00 mL所配Ba(OH)2溶液于錐形瓶中,滴加指示劑,將______(填“0.020”、“0.05”、“0.1980”或“1.5”)mol·L-1鹽酸裝入50 mL酸式滴定管,滴定至終點,記錄數據。重復滴定2次。平均消耗鹽酸V mL。
③計算Ba(OH)2·8H2O的質量分數=________(只列出算式,不做運算)。
(3)室溫下,_______(填“能”或“不能”) 配制1.0 mol·L-1 Ba(OH)2溶液。
某同學進行實驗研究時,欲配制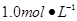 Ba(OH)2溶液,但只找到在空氣中暴露已久的Ba(OH)2·8H2O試劑(化學式量:315)。在室溫下配制溶液時發現所取試劑在水中僅部分溶解,燒杯中存在大量未溶物。為探究原因,該同學查得Ba(OH)2·8H2O在283K、293K和303K時的溶解度(g/100g H2O)分別為2.5、3.9和5.6。
Ba(OH)2溶液,但只找到在空氣中暴露已久的Ba(OH)2·8H2O試劑(化學式量:315)。在室溫下配制溶液時發現所取試劑在水中僅部分溶解,燒杯中存在大量未溶物。為探究原因,該同學查得Ba(OH)2·8H2O在283K、293K和303K時的溶解度(g/100g H2O)分別為2.5、3.9和5.6。
(1)燒杯中未溶物僅為BaCO3,理由是
(2)假設試劑由大量Ba(OH)2·8H2O和少量BaCO3組成,設計實驗方案,進行成分檢驗。在答題卡上寫出實驗步驟、預期現象和結論。(不考慮結晶水的檢驗;室溫時BaCO3飽和溶液的pH=9.6)
限選試劑及儀器:稀鹽酸、稀硫酸、NaOH溶液、澄清石灰水、pH計、燒杯、試管、帶塞導氣管、滴管

(3)將試劑初步提純后,準確測定其中Ba(OH)2·8H2O的含量。實驗如下:
①配制250ml 約 Ba(OH)2·8H2O溶液:準確稱取w克試樣,置于燒杯中,加適量蒸餾水, ,將溶液轉入 ,洗滌,定容,搖勻。
Ba(OH)2·8H2O溶液:準確稱取w克試樣,置于燒杯中,加適量蒸餾水, ,將溶液轉入 ,洗滌,定容,搖勻。
②滴定:準確量取25.00ml所配制Ba(OH)2溶液于錐形瓶中,滴加指示劑,將
(填“0.020”、“0.05”、“0.1980”或“1.5”) 鹽酸裝入50ml酸式滴定管,滴定至終點,記錄數據。重復滴定2次。平均消耗鹽酸Vml。
鹽酸裝入50ml酸式滴定管,滴定至終點,記錄數據。重復滴定2次。平均消耗鹽酸Vml。
③ 計算Ba(OH)2·8H2O的質量分數= (只列出算式,不做運算)
(4)室溫下,
(填“能”或“不能”) 配制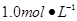 Ba(OH)2溶液。
Ba(OH)2溶液。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com