
題目列表(包括答案和解析)
 用50mL0.50mol/L鹽酸與50mL0.55mol/LNaOH溶液在如圖所示的裝置中進行中和反應.通過測定反應過程中所放出的熱量可計算中和熱.回答下列問題:
用50mL0.50mol/L鹽酸與50mL0.55mol/LNaOH溶液在如圖所示的裝置中進行中和反應.通過測定反應過程中所放出的熱量可計算中和熱.回答下列問題: 用50mL0.50mol/L鹽酸與50mL0.55mol/LNaOH溶液在如圖所示的裝置中進行中和反應.通過測定反應過程中所放出的熱量可計算中和熱.回答下列問題:
用50mL0.50mol/L鹽酸與50mL0.55mol/LNaOH溶液在如圖所示的裝置中進行中和反應.通過測定反應過程中所放出的熱量可計算中和熱.回答下列問題:| A、將溴乙烷與氫氧化鉀混合液加熱,再滴加硝酸銀溶液,觀察有沉淀生成,可證明溴乙烷中含有溴 | B、準確量取25.00 mL的液體可選用移液管、量筒或滴定管等量取 | C、在中和熱測定實驗中,為準確測得反應前后的溫差,應將已分別測得溫度的氫氧化鈉溶液與鹽酸在隔熱的容器中快速混合,并不斷攪拌,用溫度計測量混合液的最高溫度 | D、在抽濾裝置中洗滌晶體時,為減少晶體溶解損失,應使洗滌劑快速通過濾紙 |
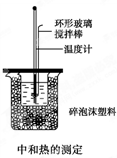 50mL 0.50mol/L鹽酸與50mL 0.55mol/L NaOH溶液在如圖所示的裝置中進行中和反應,通過測定反應過程中所放出的熱量可計算中和熱,回答下列問題:
50mL 0.50mol/L鹽酸與50mL 0.55mol/L NaOH溶液在如圖所示的裝置中進行中和反應,通過測定反應過程中所放出的熱量可計算中和熱,回答下列問題: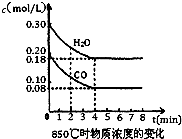 已知反應:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,生成的CO2與H2以不同的體積比混合時在合適條件下的反應可制得CH4.
已知反應:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,生成的CO2與H2以不同的體積比混合時在合適條件下的反應可制得CH4.| 1 | 2 |
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com