
題目列表(包括答案和解析)
(10分)“低碳循環(huán)”已經引起了國民的重視,試回答下列問題:
(1)煤的氣化和液化可以提高燃料的利用率。
已知25℃,101 時:
時:

則在25℃,101 時:
時: .
.
(2)高爐煉鐵是CO氣體的重要用途之一,其基本反應為: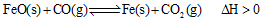 ,已知在1100℃時,該反應的化學平衡常數K=0.263。
,已知在1100℃時,該反應的化學平衡常數K=0.263。
①溫度升高,化學平衡移動后達到新的 平衡,此時平衡常數K值 (填“增大”、“減小”或“不變”);
平衡,此時平衡常數K值 (填“增大”、“減小”或“不變”);
②1100℃時測得高爐時, ,在這種情況下,該反應是否處于化學平衡狀態(tài)? (填“是”或“否”),其判斷依據是 。
,在這種情況下,該反應是否處于化學平衡狀態(tài)? (填“是”或“否”),其判斷依據是 。
③目前工業(yè)上可用 來生產燃料甲醇
來生產燃料甲醇 ,有關反應為:
,有關反應為: 。現向體積為1L的密閉容器中,充入1mol
。現向體積為1L的密閉容器中,充入1mol 和3mol
和3mol ,反應過程中測得
,反應過程中測得 和
和 (g)的濃度隨時間的變化如圖所示。
(g)的濃度隨時間的變化如圖所示。
①從反應開始到平衡,氫氣的平均反應速率 ;
;
②下列措施能使 增大的是
增大的是  (填符號)。
(填符號)。
| A.升高溫度 |
B.再充入 |
C.再充入 |
D.將 (g)從體系中分離 (g)從體系中分離 |
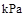 時:
時: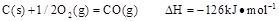

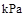 時:
時: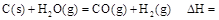 .
.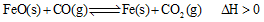 ,已知在1100℃時,該反應的化學平衡常數K=0.263。
,已知在1100℃時,該反應的化學平衡常數K=0.263。 平衡,此時平衡常數K值 (填“增大”、“減小”或“不變”);
平衡,此時平衡常數K值 (填“增大”、“減小”或“不變”);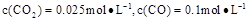 ,在這種情況下,該反應是否處于化學平衡狀態(tài)? (填“是”或“否”),其判斷依據是 。
,在這種情況下,該反應是否處于化學平衡狀態(tài)? (填“是”或“否”),其判斷依據是 。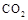 來生產燃料甲醇
來生產燃料甲醇 ,有關反應為:
,有關反應為: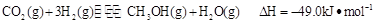 。現向體積為1L的密閉容器中,充入1mol
。現向體積為1L的密閉容器中,充入1mol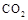 和3mol
和3mol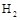 ,反應過程中測得
,反應過程中測得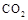 和
和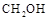 (g)的濃度隨時間的變化如圖所示。
(g)的濃度隨時間的變化如圖所示。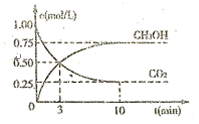
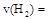 ;
;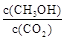 增大的是
增大的是  (填符號)。
(填符號)。| A.升高溫度 |
B.再充入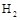 |
C.再充入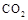 |
D.將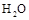 (g)從體系中分離 (g)從體系中分離 |
“低碳循環(huán)”引起各國的高度重視,已知煤、甲烷等可以與水蒸氣反應生成以CO和H2為主的合成氣,合成氣有廣泛應用。試回答下列問題:
(1)高爐煉鐵是CO氣體的重要用途之一,其基本反應為:
FeO(s)+CO(g) ![]() Fe(s)+CO2(g) ΔH >0
Fe(s)+CO2(g) ΔH >0
已知在1100℃時,該反應的化學平衡常數K=0.263。
①溫度升高,化學平衡移動后達到新的平衡,此時平衡常數K值__________(填“增大”、“減小”或“不變”);
②1100℃時測得高爐中,c(CO2)=0.025mol·L-1,c(CO)=0.1 mol·L-1,則在這種情況下,該反應向_______進行(填“左”或“右”),判斷依據是
。
(2)一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO)。
已知:2CO(g) + O2(g)=2CO2(g) ΔH =–566 kJ·mol―1
2H2O(g) =2H2(g) + O2(g) ΔH =+484 kJ·mol―1
CH3OH(g) + 1/2O2(g)=CO2(g) + 2H2(g) ΔH =–192.9 kJ·mol―1
請寫出CO與H2在一定條件下反應生成CH3OH(g)的熱化學方程式
。
(3)目前工業(yè)上也可用CO2來生產燃料甲醇,有關反應為:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH =-49.0 kJ·mol-1,現向體積為1 L的密閉 容器中,充入1mol CO2和3mol H2,反應過程中測得CO2和CH3OH(g)的濃度隨時間的變化如圖所示。
CH3OH(g)+H2O(g) ΔH =-49.0 kJ·mol-1,現向體積為1 L的密閉 容器中,充入1mol CO2和3mol H2,反應過程中測得CO2和CH3OH(g)的濃度隨時間的變化如圖所示。
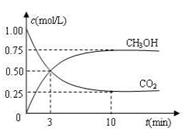
①從反應開始到平衡,氫氣的平均反應速率v(H2)=_______ _;
②反應達到平衡后,下列措施能使![]() 增大的是______(填符號)。
增大的是______(填符號)。
A.升高溫度 B.再充入H2 C.再充入CO2
D.將H2O(g)從體系中分離 E.充入He(g)
“低碳循環(huán)”引起各國的高度重視,已知煤、甲烷等可以與水蒸氣反應生成以CO和H2為主的合成氣,合成氣有廣泛應用。試回答下列問題:
(1)高爐煉鐵是CO氣體的重要用途之一,其基本反應為:
FeO(s)+CO(g)  Fe(s)+CO2(g) ΔH >0
Fe(s)+CO2(g) ΔH >0
已知在1100℃時,該反應的化學平衡常數K=0.263。
①溫度升高,化學平衡移動后達到新的平衡,此時平衡常數K值__________(填“增大”、“減小”或“不變”);
②1100℃時測得高爐中,c(CO2)=0.025mol·L-1,c(CO)=0.1 mol·L-1,則在這種情況下,該反應向_______進行(填“左”或“右”),判斷依據是
。
(2)一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO)。
已知:2CO(g) + O2(g)=2CO2(g) ΔH =–566 kJ·mol―1
2H2O(g) =2H2(g) + O2(g) ΔH =+484 kJ·mol―1
CH3OH(g) + 1/2O2(g)=CO2(g) + 2H2(g) ΔH =–192.9 kJ·mol―1
請寫出CO與H2在一定條件下反應生成CH3OH(g)的熱化學方程式
。
(3)目前工業(yè)上也可用CO2來生產燃料甲醇,有關反應為:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
ΔH =-49.0
kJ·mol-1,現向體積為1 L的密閉 容器中,充入1mol CO2和3mol H2,反應過程中測得CO2和CH3OH(g)的濃度隨時間的變化如圖所示。
CH3OH(g)+H2O(g)
ΔH =-49.0
kJ·mol-1,現向體積為1 L的密閉 容器中,充入1mol CO2和3mol H2,反應過程中測得CO2和CH3OH(g)的濃度隨時間的變化如圖所示。

①從反應開始到平衡,氫氣的平均反應速率v(H2)=_______ _;
②反應達到平衡后,下列措施能使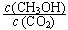 增大的是______(填符號)。
增大的是______(填符號)。
A.升高溫度 B.再充入H2 C.再充入CO2
D.將H2O(g)從體系中分離 E.充入He(g)
“低碳循環(huán)”引起各國的高度重視,已知煤、甲烷等可以與水蒸氣反應生成以CO和H2為主的合成氣,合成氣有廣泛應用。試回答下列問題:
(1)高爐煉鐵是CO氣體的重要用途之一,其基本反應為:FeO(s)+CO(g)![]() Fe(s)+CO2(g) ΔH>0。已知在1100℃時,該反應的化學平衡常數K=0.263。
Fe(s)+CO2(g) ΔH>0。已知在1100℃時,該反應的化學平衡常數K=0.263。
①溫度升高,化學平衡移動后達到新的平衡,此時平衡常數K值 (填“增大”、“減小”或“不變”);
②1100 ℃時測得高爐中,c(CO2)=0.025 mol·L-1,c(CO)=0.1 mol·L-1,則在這種情況下,該反應向 進行(填“左”或“右”),判斷依據是 。
(2)目前工業(yè)上也可用CO2來生產燃料甲醇,有關反應:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,現向體積為1 L的密閉容器中,充入1 mol CO2和3 mol H2,反應過程中測得CO2和CH3OH(g)的濃度隨時間的變化如圖所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,現向體積為1 L的密閉容器中,充入1 mol CO2和3 mol H2,反應過程中測得CO2和CH3OH(g)的濃度隨時間的變化如圖所示。
①該反應的化學平衡常數表達式為 ;
②反應達到平衡時,氫氣的轉化率 α(H2)= ;
③反應達到平衡后,下列措施能使![]() 增大的是 (填序號)。
增大的是 (填序號)。
A.升高溫度 B.再充入H2 C.再充入CO2
D.將H2O(g)從體系中分離 E.充入He(g)
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com