
題目列表(包括答案和解析)

| ||
| ||

(1)二氧化鈦在上述反應中的作用是_______________________________________。
(2)如果用NaClO處理含NaCl的廢液,則可能生成另外兩種鹽(毒性降解),試寫出此反應的化學方程式:_____________________________________________。(其中N均為-3價)
此反應中被氧化的元素是______________。
(3)氰酸鹽再與次氯酸鹽作用降解產生的無毒氣體有哪些?
____________________________________________________________________。
寫出可能發生的離子方程式________________________________________________。
有氰化物的廢水危害極大,能毒殺各種魚類和水生物。CN-濃度在0.01—0.04 mg·L-1時就有強烈的毒殺作用,處理含有氰化物的工業廢水的方法之一是:使CN-被氧化轉變為低毒的CNO-(其毒性僅為氰化物的千分之一),一般轉化為氰酸鹽(如NaCNO)。氧化劑常用次氯酸鹽,同時還可降解產生無毒氣體。近期研究表明,在光的作用下,在某些懸浮小粒表面和溶液界面可發生明顯的氧化還原反應,很快降解毒性,如在二氧化鈦(TiO2)表面上可以降解氰化物等有毒物。
(1)二氧化鈦在上述反應中的作用是______________________________________________。
(2)如果用NaClO處理含NaCl的廢液,則可能生成另外兩種鹽(毒性降解),試寫出此反應的化學方程式:_____________________________________________。(其中N均為-3價)
此反應中被氧化的元素是___________________________。
(3)氰酸鹽再與次氯酸鹽作用降解產生的無毒氣體有哪些?
______________________________________________________________________________。
寫出可能發生的離子方程式______________________________________________________。
| |||||||||||||||||||||||||
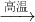 2AlN+3CO
2AlN+3CO
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com