
題目列表(包括答案和解析)
黃銅礦(CuFeS2)是煉鋼和煉銅的主要原料.在高溫下灼燒生成二氰化二鐵和氧化銅。三氧化二鐵和氧化亞銅都是紅色粉末.常用作顏料。某學校化學興趣小組通過實驗米探究一紅色粉末是Fe2O3、Cu2O或兩者的混合物。探究過程如下:
【查閱資料】Cu2O是一種堿性氧化物.溶于稀硫酸生成Cu和CuSO4,在空氣中加熱生成CuO。
【提出假設】
假設1:紅色粉末是Fe2O3。假設2:紅色粉末是Cu2O。假設3:紅色粉末是Fe2O3和Cu2O的混合物。
【設計探究實驗】
取少量粉末放入足量稀硫酸中.在所得溶液中再滴加KSCN試劑。
(1)若假設1成立,則實驗現象是??????? 。
(2)滴加KSCN試劑后溶液不變紅色.某同學認為原同體粉末中一定不含三氧化二鐵。你認為這種說法合理嗎???? 。簡述你的理由(不需寫出反應的化學方程式):?????????????? 。
(3)若固體粉末未完全溶解,仍然有固體存在.滴加KSCN試劑時溶液不變紅色.則證明原固體粉末是??? ,寫出發生的氧化還原反應的離子方程式:????? 。
【探究延伸】
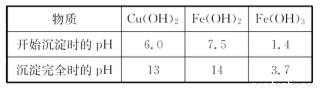
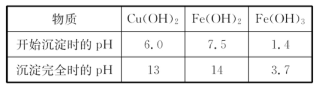
(4)經過實驗分析.確定紅色粉末為Fe2O3和Cu2O的混合物。實驗小組欲利用該紅色粉末制取較純凈的膽礬(CuSO4·5H2O)。經過查閱資料得知.在溶液中通過調節溶液的酸堿性而使Cu2+、Fe2+、Fe3+分別生成沉淀的pH如下:
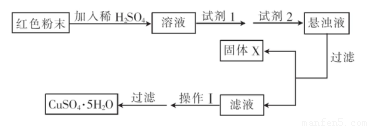
實驗小組設汁如下實驗方案:
①試劑1為??? .試劑2為??????? . (填字母)
A.氯水????? B.H2O2???? C.NaOH??? D.CuO
②固體X的化學式為???????? 。
③操作II為?????????????? 。
黃銅礦(CuFeS2)是煉鋼和煉銅的主要原料.在高溫下灼燒生成二氰化二鐵和氧化銅。三氧化二鐵和氧化亞銅都是紅色粉末.常用作顏料。某學校化學興趣小組通過實驗米探究一紅色粉末是Fe2O3、Cu2O或兩者的混合物。探究過程如下:
【查閱資料】Cu2O是一種堿性氧化物.溶于稀硫酸生成Cu和CuSO4,在空氣中加熱生成CuO。
【提出假設】
假設1:紅色粉末是Fe2O3。假設2:紅色粉末是Cu2O。假設3:紅色粉末是Fe2O3和Cu2O的混合物。
【設計探究實驗】
取少量粉末放入足量稀硫酸中.在所得溶液中再滴加KSCN試劑。
(1)若假設1成立,則實驗現象是 。
(2)滴加KSCN試劑后溶液不變紅色.某同學認為原同體粉末中一定不含三氧化二鐵。你認為這種說法合理嗎? 。簡述你的理由(不需寫出反應的化學方程式): 。
(3)若固體粉末未完全溶解,仍然有固體存在.滴加KSCN試劑時溶液不變紅色.則證明原固體粉末是 ,寫出發生的氧化還原反應的離子方程式: 。
【探究延伸】
(4)經過實驗分析.確定紅色粉末為Fe2O3和Cu2O的混合物。實驗小組欲利用該紅色粉末制取較純凈的膽礬(CuSO4·5H2O)。經過查閱資料得知.在溶液中通過調節溶液的酸堿性而使Cu2+、Fe2+、Fe3+分別生成沉淀的pH如下:
實驗小組設汁如下實驗方案:
①試劑1為 .試劑2為 . (填字母)
| A.氯水 | B.H2O2 | C.NaOH | D.CuO |

| A.氯水 | B.H2O2 | C.NaOH | D.CuO |
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com