
題目列表(包括答案和解析)
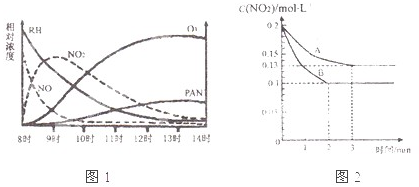
| C4(NO2)C(O2) |
| C2(N2O5) |
| C4(NO2)C(O2) |
| C2(N2O5) |
控制、治理氮氧化物對大氣的污染是改善大氣質量的重要方面。
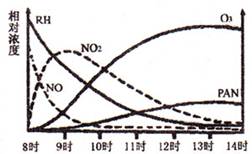 (1)光化學煙霧白天生成,傍晚消失,其主要成分為RH(烴)、NO、NO2、O3、PAN(CH3COOONO2),某地早上至中午這些物質的相對濃度變化如右圖所示,則下列敘述合理的是 。(填字母)
(1)光化學煙霧白天生成,傍晚消失,其主要成分為RH(烴)、NO、NO2、O3、PAN(CH3COOONO2),某地早上至中午這些物質的相對濃度變化如右圖所示,則下列敘述合理的是 。(填字母)
a.早上8時交通繁忙期,光化學煙霧的主要成分為RH、NO
b.14時,光化學煙霧的主要成分為O3、PAN
c.PAN、O3由RH和NO直接反應生成
d.PAN直接由O3轉化生成
(2)火力發電廠的燃煤排煙中含大麓的氮氧化物(NOx),可利用甲烷和NOx一定條件下反應消除其污染,則CH4與NO2反應的化學方程式為 。
(3)在一密閉容器中發生反應2NO2![]() 2NO+O2,反應過程中NO2的濃度隨時間變化的情況如右下圖所示。請回答:
2NO+O2,反應過程中NO2的濃度隨時間變化的情況如右下圖所示。請回答:
① 依曲線A,反應在前3 min內氧氣的平均反應速率為 。
② 若曲線A、B分別表示的是該反應在某不同條件下的反應情況,則此條件是 (填“濃度”、“壓強”、“溫度”或“催化劑”)。
③ 曲線A、B分剮對應的反應平衡常數的大小關系是![]()
![]() 。(填“>”、“<”或“=”)
。(填“>”、“<”或“=”)
(4)一定溫度下,在匭容密閉容器中N2O5可發生下列反應:
2N2O5(g)![]() 4NO2(g)+O2(g) Ⅰ
4NO2(g)+O2(g) Ⅰ
2NO2(g)![]() 2NO(g)+O2(g) Ⅱ
2NO(g)+O2(g) Ⅱ
則反應Ⅰ的平衡常數表達式為 。若達平衡時,![]() (NO2)=0.4 mol?L
(NO2)=0.4 mol?L![]() ,
,![]() (O2)=1.3 mol?L
(O2)=1.3 mol?L![]() ,則反應Ⅱ中NO2的轉化率為 ,N2O5(g)的起始濃度應不低于 mo1?L
,則反應Ⅱ中NO2的轉化率為 ,N2O5(g)的起始濃度應不低于 mo1?L![]() 。
。
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com