
題目列表(包括答案和解析)
| ||
| ||
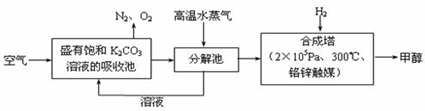
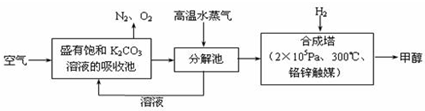
(14分)最近科學家提出“綠色自由”構想:把空氣吹入碳酸鉀溶液,然后再把CO2從溶液中提取出來,經化學反應后使空氣中的CO2轉變為可再生燃料甲醇。“綠色自由”構想技術流程如下:
(1)在合成塔中,若有2.2kgCO2與足量H2恰好完全反應,生成氣態的水和甲醇,可放出2473.5kJ的熱量,試寫出合成塔中發生反應的熱化學方程式 。
(2)①上述合成反應具有一定的可逆性,從平衡移動原理分析,低溫有利于原料氣的轉化,而實際生產中采用300°C的溫度,其原因是 。
②“綠色自由”構想技術流程中常包括物質和能量的“循環利用”,上述流程中能體現“循環利用”的除碳酸鉀溶液外,還包括 。
③下列措施中能使n(CH3OH)/n(CO2)增大的是___________。
A.升高溫度 B.充入He(g),使體系壓強增大
C.將H2O(g)從體系中分離 D.再充入1mol CO2和3mol H2
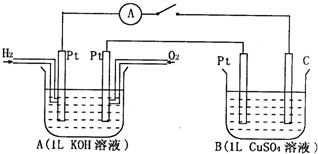
(3)甲醇可制作燃料電池。寫出以氫氧化鉀為電解質的甲醇燃料電池負極反應式 。當電子轉移的物質的量為 時,參加反應的氧氣的體積是6.72L(標準狀況下)。
(4)常溫下,0.1 mol/L KHCO3溶液的pH大于8,則溶液中各種離子濃度由大到小的順序為:
。
(14分)最近科學家提出“綠色自由”構想:把空氣吹入碳酸鉀溶液,然后再把CO2從溶液中提取出來,經化學反應后使空氣中的CO2轉變為可再生燃料甲醇。“綠色自由”構想技術流程如下:

(1)在合成塔中,若有2.2kgCO2與足量H2恰好完全反應,生成氣態的水和甲醇,可放出2473.5kJ的熱量,試寫出合成塔中發生反應的熱化學方程式 。
(2)①上述合成反應具有一定的可逆性,從平衡移動原理分析,低溫有利于原料氣的轉化,而實際生產中采用300°C的溫度,其原因是 。
②“綠色自由”構想技術流程中常包括物質和能量的“循環利用”,上述流程中能體現“循環利用”的除碳酸鉀溶液外,還包括 。
③下列措施中能使n(CH3OH)/n(CO2)增大的是___________。
A.升高溫度 B.充入He(g),使體系壓強增大
C.將H2O(g)從體系中分離 D.再充入1mol CO2和3mol H2
(3)甲醇可制作燃料電池。寫出以氫氧化鉀為電解質的甲醇燃料電池負極反應式 。當電子轉移的物質的量為 時,參加反應的氧氣的體積是6.72L(標準狀況下)。
(4)常溫下,0.1 mol/L KHCO3溶液的pH大于8,則溶液中各種離子濃度由大到小的順序為:
。
說明:
1. 本答案供閱卷評分使用,試題的參考解答是用來說明評分標準的,考生如按其他方法或步驟解答,正確的同樣給分;有錯的,根據錯誤的性質,參照評分標準中相應的規定評分。
2. 化學專用名詞中出現錯別字、元素符號有錯誤,都要參照評分標準扣分。
3. 化學方程式、離子方程式未配平的,都不給分。
4. 計算只有最后答案而無演算過程的,不給分。
第Ⅰ卷(選擇題,共50分)
一、選擇題(本題包括25小題,每小題2分,共50分。每小題只有一個選項符合題意)
1. D 2. B 3. C 4. D 5. B 6. D 7. C 8. A 9. A 10. C 11. C 12. B 13. B 14. A
15. D 16. D 17. B 18. A 19. A 20. C 21. C 22. A 23. B 24. C 25. D
第Ⅱ卷(非選擇題,共50分)
二、填空題(本題包括6小題,每空1分,共25分)
26.(4分) > > 10-7 mol?L-1 10-14
27.(6分)2 失去2 3 FeS Fe+Cu2+===Fe2++Cu 2Fe+3Cl2點燃=====2FeCl3
28.(4分)→ ← ← ―
 29.(2分)正 氧化
29.(2分)正 氧化
 30.(5分)(1)Al 3 ⅢA (2)鈉
30.(5分)(1)Al 3 ⅢA (2)鈉
31.(4分)
三、簡答題(本題包括3小題,共15分)
32.(共7分,每空1分)(1)2Al+Fe2O3高溫=====2Fe+Al2O3 鋁(或Al)
(2)大量氣泡 2H2O2MnO2======2H2O+O2↑
(3)紅 變深 增大任何一種反應物的濃度,都促使化學平衡向正反應方向移動
33.(共4分,每空1分)酸 Fe3++3H2O Fe(OH)3+3H+
鹽酸(或HCl)
Fe(OH)3+3H+
鹽酸(或HCl)
抑制Ag+ 的水解,防止溶液變渾濁
34.(共4分)(1)氣體顏色加深(1分) 氣體顏色變淺(1分) (2)升高溫度,化學平衡向吸熱反應方向移動;降低溫度,平衡向放熱反應方向移動(2分)
四、計算題(本題包括2小題,共10分)
 35. 解:HNO3+KOH===KNO3+H2O ……………………………………………(1分)
35. 解:HNO3+KOH===KNO3+H2O ……………………………………………(1分)
c(HNO3)?V[HNO3(aq)]=c(KOH)?V[KOH(aq)] ……………………………(1分)
c(HNO3)===0.5018 mol/L (2分)
答:這種HNO3溶液的物質的量濃度為0.5018 mol/L。
36. 解:合金粉末與過量的NaOH溶液混合,只有Al與NaOH反應。
2Al+2NaOH+2H2O===2NaAlO2+3H2↑ 
2×27 g
3×22.4 L
m(Al)
3.36 L …………………………………(2分)
m(Al)= =2.7 g ……………………………………………(2分)
=2.7 g ……………………………………………(2分)
合金中鎂的質量分數w(Mg)=×100 %=32.5 % ………………(2分)
答:合金中鎂的質量分數為32.5 % 。

湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com