
題目列表(包括答案和解析)
碳及其化合物有廣泛的用途。
(1)將水蒸氣通過紅熱的碳即可產生水煤氣反應為
C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.3 kJ·mol-1,
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1,
以上反應達到平衡后,在體積不變的條件下,以下措施有利于提高H2O的平衡轉化率的是________。(填序號)
| A.升高溫度 | B.增加碳的用量 | C.加入催化劑 | D.用CO吸收劑除去CO |
 2CO(g) ΔH=+172.5 kJ·mol-1,則CO(g)+H2O(g)
2CO(g) ΔH=+172.5 kJ·mol-1,則CO(g)+H2O(g) CO2(g)+H2(g)的焓變ΔH=________。
CO2(g)+H2(g)的焓變ΔH=________。 CH3OH(g)。甲醇是一種燃料,可利用甲醇設計一個燃料電池,用稀硫酸作電解質溶液,多孔石墨作電極,該電池負極反應式為______________________________________。
CH3OH(g)。甲醇是一種燃料,可利用甲醇設計一個燃料電池,用稀硫酸作電解質溶液,多孔石墨作電極,該電池負極反應式為______________________________________。 CO2(g)+H2(g)。得到如下數據:
CO2(g)+H2(g)。得到如下數據:| 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所 需時間/min | ||
| H2O | CO | H2 | CO | | |
| 900 | 1.0 | 2.0 | 0.4 | 1.6 | 3.0 |
 2NH3(g) ΔH=-92.4 kJ·mol-1。實驗室模擬化工生產,分別在不同實驗條件下反應,N2濃度隨時間變化如圖甲所示。
2NH3(g) ΔH=-92.4 kJ·mol-1。實驗室模擬化工生產,分別在不同實驗條件下反應,N2濃度隨時間變化如圖甲所示。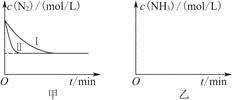
已知反應
:CO(g)+H2O(g)(1)
將1 mol CO和1 mol H2O(g)充入某固定容積的反應器,在某溫度下達到平衡:此時有2/3的CO轉化為CO2.則該反應平衡常數的表達式為________,此溫度下平衡常數為________.(2)
若在相同條件下,向該容器中充入1 mol CO2、1 mol H2,則達到平衡時與(1)相比較,平衡應________移動(填“向正反應方向”、“向逆反應方向”或“不”),此時平衡混合氣中CO2的體積分數約是下列各值中的________(填編號)A.22.2%
B.27.55%
C.33.3%
D.36.8%
(3)
若在相同條件下,向該容器中充入1 mol CO2、1 mol H2和1 mol H2O(g),則達到平衡時與(1)相比較,則下列說法中正確的是________(填序號)①生成物的產量一定增加
②反應物的濃度一定降低
③反應物的轉化率一定增加
④
CO在平衡混合氣中的百分含量一定降低(6分)碳和碳的化合物在生產、生活中的應用非常廣泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一種理想,更是一種值得期待的新的生活方式。
(1) 甲烷燃燒放出大量的熱,可作為能源用于人類的生產和生活。
已知:①2CH4(g)+3O2(g)=2CO(g)+4H2O(l) △H1= —1214 kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H2= —566 kJ/mol
則表示甲烷燃燒熱的熱化學方程式 。
(2) 將兩個石墨電極插入KOH溶液中,向兩極分別通入CH4和O2,構成甲烷燃料電池。其負極電極反應式是: 。
(3)某同學利用甲烷燃料電池設計了一種電解法制取Fe(OH)2的實驗裝置(如下圖所示),通電后,溶液中產生大量的白色沉淀,且較長時間不變色。下列說法中正確的是 (填序號)
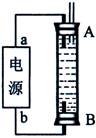
A.電源中的a一定為正極,b一定為負極
B.可以用NaCl溶液作為電解液
C.A、B兩端都必須用鐵作電極
D.陰極發生的反應是:2H+ + 2e-= H2↑
(4)將不同量的CO(g)和H2O(g)分別通入體積為2L的恒容密閉容器中,進行反應:
CO(g)+H2O(g)===CO2(g)+H2(g),得到如下三組數據:
|
實驗組 |
溫度/℃ |
起始量/mol |
平衡量/mol |
達到平衡所需時間/min |
|
|
H2O |
CO |
CO2 |
|||
|
1 |
650 |
2 |
4 |
1.6 |
5 |
|
2 |
900 |
1 |
2 |
0.4 |
3 |
|
3 |
900 |
1 |
2 |
0.4 |
1 |
①實驗1中,以v (H2)表示的平均反應速率為 。
②實驗3跟實驗2相比,改變的條件可能是 (答一種情況即可)。
碳和碳的化合物在生產、生活中的應用非常廣泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一種理想,更是一種值得期待的新的生活方式。
(1)甲烷燃燒放出大量的熱,可作為能源用于人類的生產和生活。
已知:①2CH4(g)+3O2(g)=2CO(g)+4H2O(l) △H=" —1214" kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H=" —566" kJ/mol
則表示甲烷燃燒熱的熱化學方程式 。
(2) 將兩個石墨電極插入KOH溶液中,向兩極分別通入CH4和O2,構成甲烷燃料電池。其負極電極反應式是: 。
(3)某同學利用甲烷燃料電池設計了一種電解法制取Fe(OH)2的實驗裝置(如下圖所示),通電后,溶液中產生大量的白色沉淀,且較長時間不變色。下列說法中正確的是 (填序號)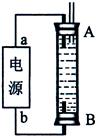
A.電源中的a一定為正極,b一定為負極
B.可以用NaCl溶液作為電解液
C.A、B兩端都必須用鐵作電極
D.陰極發生的反應是:2H+ + 2e-= H2↑
(4)將不同量的CO(g)和H2O(g)分別通入體積
為2L的恒容密閉容器中,進行反應:
CO(g)+H2O(g)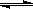 CO2(g)+H2(g),得到如下三組數據:
CO2(g)+H2(g),得到如下三組數據:
| 實驗組 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | |
| H2O | CO | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 3 |
| 3 | 900 | 1 | 2 | 0.4 | 1 |

| 時間 \CO轉化率 \溫度 |
1小時 | 2小時 | 3小時 | 4小時 |
| T1 | 30% | 50% | 80% | 80% |
| T2 | 35% | 60% | a1 | a2 |
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com