
題目列表(包括答案和解析)
(15分)硫酸廠用煅燒黃鐵礦(FeS2)來制取硫酸,實驗室利用硫酸廠燒渣(主要成分是Fe2O3及少量FeS、SiO2)制備綠礬.
⑴SO2和O2反應制取SO3的反應原理為:2SO2+O2 2SO3,在一密閉容器中一定時間內達到平衡.
2SO3,在一密閉容器中一定時間內達到平衡.
①該反應的平衡常數表達式為: .
②該反應達到平衡狀態的標志是 .
A.v(SO2)=v(SO3) B.混合物的平均相對分子質量不變
C.混合氣體質量不變 D.各組分的體積分數不變
⑵某科研單位利用原電池原理,用SO2和O2來制備硫酸,裝置如圖,電極為多孔的材料能吸附氣體,同時也能使氣體與電解質溶液充分接觸.
①B電極的電極反應式為 ;
②溶液中H+的移動方向由 極到 極;(用A、B表示)
⑶測定綠礬產品中含量的實驗步驟:
a.稱取5.7 g產品,溶解,配成250 mL溶液
b.量取25 mL待測液于錐形瓶中
c.用硫酸酸化的0.01 mol/L KMnO4溶液滴定至終點,消耗KMnO4溶液體積40 mL
根據上述步驟回答下列問題:
①滴定時發生反應的離子方程式為(完成并配平離子反應方程式).
Fe2++  + —— Fe3++ Mn2++
+ —— Fe3++ Mn2++
②用硫酸酸化的KMnO4滴定終點的標志是 .
③計算上述產品中FeSO4·7H2O的質量分數為 .
(15分)硫酸廠用煅燒黃鐵礦(FeS2)來制取硫酸,實驗室利用硫酸廠燒渣(主要成分是Fe2O3及少量FeS、SiO2)制備綠礬.
⑴SO2和O2反應制取SO3的反應原理為:2SO2+O2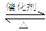 2SO3,在一密閉容器中一定時間內達到平衡.
2SO3,在一密閉容器中一定時間內達到平衡.
①該反應的平衡常數表達式為: .
②該反應達到平衡狀態的標志是 .
A.v(SO2)=v(SO3) B.混合物的平均相對分子質量不變
C.混合氣體質量不變 D.各組分的體積分數不變
⑵某科研單位利用原電池原理,用SO2和O2來制備硫酸,裝置如圖,電極為多孔的材料能吸附氣體,同時也能使氣體與電解質溶液充分接觸.
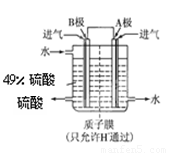
①B電極的電極反應式為 ;
②溶液中H+的移動方向由 極到 極;(用A、B表示)
⑶測定綠礬產品中含量的實驗步驟:
a.稱取5.7 g產品,溶解,配成250 mL溶液
b.量取25 mL待測液于錐形瓶中
c.用硫酸酸化的0.01 mol/L KMnO4溶液滴定至終點,消耗KMnO4溶液體積40 mL
根據上述步驟回答下列問題:
①滴定時發生反應的離子方程式為(完成并配平離子反應方程式).
Fe2++ 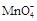 +
——
Fe3++ Mn2++
+
——
Fe3++ Mn2++
②用硫酸酸化的KMnO4滴定終點的標志是 .
③計算上述產品中FeSO4·7H2O的質量分數為 .
| c(Cr2O72-) |
| c2(CrO42-)?c2(H+) |
| c(Cr2O72-) |
| c2(CrO42-)?c2(H+) |
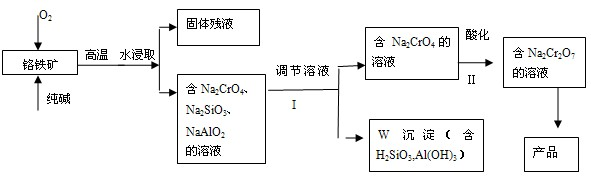
重鉻酸鈉(Na2Cr2O7)廣泛用于合成顏料、媒染劑等。以鉻鐵礦(主要成分為Cr2O3還含有FeO、Al2O3、SiO2等雜質)為原料制取重鉻酸鈉的流程圖如下:
 請回答下列問題。
請回答下列問題。
(1)若I中只用一種試劑調節溶液的pH,應選用___________(填標號)。
A.稀硫酸 B.氧化鈉固體 C.氫氧化鉀溶液
(2)I中,調節溶液pH后,如果溶液的pH過小,可能導致W沉淀部分溶解,原因是
_______________________________________________________ (用離子方程式表示)。
(3)Ⅱ中,Na2CrO4轉化為Na2Cr2O7的離子反應如下: 2CrO42- (黃色)+2H+![]() Cr2O72- (橙紅色)+H2O
Cr2O72- (橙紅色)+H2O
①該反應________氧化還原反應(填“是”或“不是”),反應的平衡常數表達式 K=__________。
②若往Na2Cr2O7溶液(橙紅色)中加入足量NaOH固體,溶液_______ (填標號)。
A.變黃色 B.顏色不變 C.橙紅色變深
③已知:25℃時,Ag2CrO4的Ksp=1.12×10-12,Ag2Cr2O7的Ksp=2×10-7。25℃時,往Na2Cr2O7溶液中加入AgNO3溶液,最終只生成一種磚紅色沉淀,該沉淀的化學式是_____________________。
重鉻酸鈉(Na2Cr2O7)廣泛用于合成顏料、媒染劑等.以鉻鐵礦(主要成分為Cr2O3,還含有FeO,Al2O3,SiO2等雜質)為原料制取重鉻酸鈉的流程圖如下:
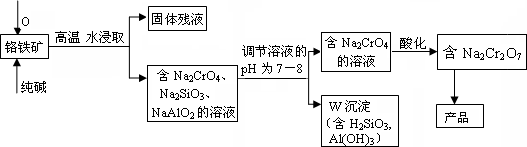
請回答下列問題:
(1)若步驟Ⅰ中只用一種試劑調節溶液的pH,應選用________(填標號).
A.稀硫酸
B.氫氧化鈉固體
C.氫氧化鉀溶液
(2)步驟Ⅰ中,調節溶液pH后,如果溶液的pH過小,可能導致W沉淀部分溶解,原因是:________(用離子方程式表示).
(3)步驟Ⅱ中,Na2CrO4轉化為Na2Cr2O7的離子反應如下:
2CrO42-(黃色)+2H+ Cr2O72-(橙紅色)+H2O
Cr2O72-(橙紅色)+H2O
①該反應________氧化還原反應(填“是”或“不是”),反應的平衡常數表達式:K=________.
②若向Na2Cr2O7溶液(橙紅色)中加入足量的NaOH固體,溶液________(填標號)
A.變黃色
B.顏色不變
C.橙紅色溶液
③已知:25℃時,Ag2CrO4的Ksp=1.12×10-12,Ag2Cr2O7的Ksp=2×10-7
25℃時,向Na2Cr2O7溶液中加入AgNO3溶液,最終只生成一種磚紅色沉淀,該沉淀的化學式是________.
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com